Uterine Sarkome bezeichnen eine heterogene Gruppe insgesamt seltener Malignome der Uterusmuskulatur oder des uterinen Bindegewebes. Die Inzidenz ist ca. 1,5 (Kaukasier) bis 3 (Afro-Amerikaner)/100.000 Einwohner.
S2k-Leitlinie: Uterine Sarkome
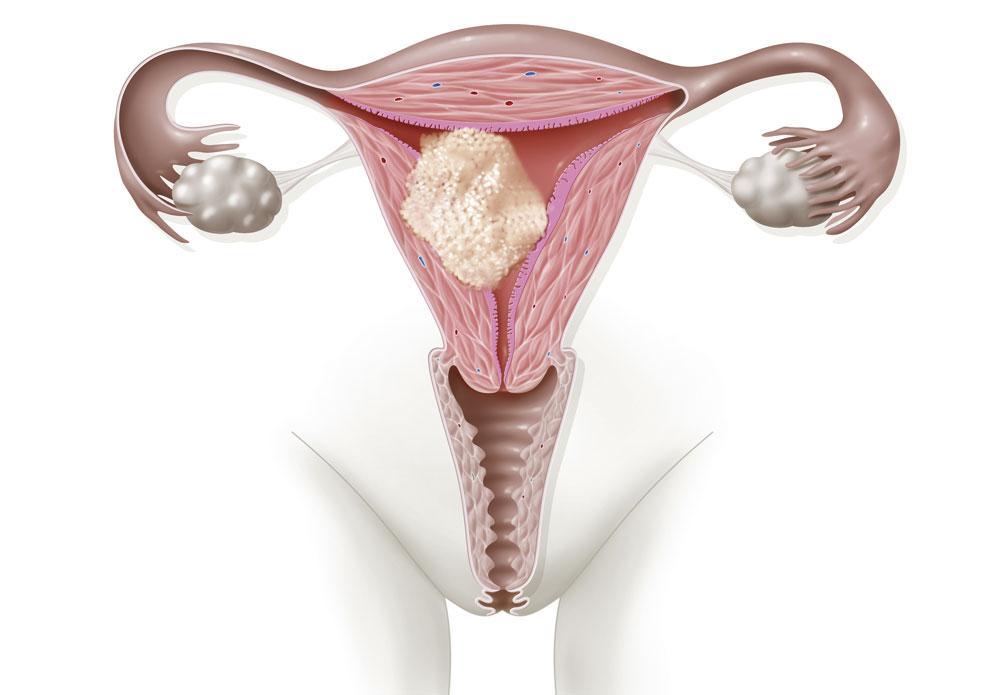 Uterine Sarkome
Uterine Sarkome
Die Tumortypisierung erfolgt nach der WHO, die Stadieneinteilung nach der FIGO- bzw. TNM-Klassifikation [1]. In der WHO-Klassifikation sind folgende Entitäten als maligne mesenchymale Tumoren bzw. maligne gemischte epithelial-mesenchymale Tumoren aufgeführt:
» Leiomyosarkome (LMS),
» Low-grade endometriale Stromasarkome (LG-ESS),
» High-grade endometriale Stromasarkome (HG-ESS),
» Undifferenzierte uterine Sarkome (UUS),
» (Adenosarkome)
» (Rhabdomyosarkome)
» (PECome – perivascular epitheloid cell tumor, maligne Variante).
Neben den extrem seltenen Formen (Adenosarkome, Rhabdomyosarkom, PECome, etc.), bezieht sich dieser Artikel auf das spezifische Management der häufigeren Entitäten (LMS, LG-ESS, HG-ESS und UUS).
Am häufigsten finden sich Leiomyosarkome mit 60 bis 70 Prozent der uterinen Sarkome bzw. ein bis zwei Prozent aller uterinen Malignome, gefolgt von den Low-grade ESS und den High-grade ESS bzw. den undifferenzierten uterinen Sarkomen mit jeweils ca. zehn Prozent der uterinen Sarkome.
Das mittlere Erkrankungsalter der uterinen Sarkome liegt abhängig vom Tumortyp bei 50 bis 70 Jahren. Als Risikofaktoren wurden eine vorausgegangene Strahlentherapie des Beckens und die Einnahme von Tamoxifen identifiziert. Darüber hinaus ist bei Frauen afrikanischer Abstammung die Inzidenz an uterinen Sarkomen um das zwei- bis dreifache höher als bei Asiatinnen oder Frauen europäischer Abstammung.
Die in früheren Klassifikationen gleichfalls als uterine Sarkome bezeichneten Karzinosarkome (auch als Maligne Müllersche Mischtumoren bezeichnet) werden nicht mehr den Uterussarkomen, sondern den Karzinomen des Uterus zugerechnet. Da diese Tumorentität allerdings bisher in anderen Empfehlungen nur unzureichend abgebildet ist, wird diese hier mit aufgeführt.
Leider gibt es keine spezifischen Symptome für uterine Sarkome. Als suspekt gilt der „schnell wachsende Uterus“ bei niedrigen Östrogenspiegeln in der Postmenopause. Aufgrund der fehlenden spezifischen Symptomatik wird in der Mehrzahl der Fälle die Diagnose entweder als Zufallsbefund am Hysterektomie-Präparat gestellt oder aber erst in fortgeschrittenen Stadien durch eine entsprechende sekundäre Begleitsymptomatik (zum Beispiel Dyspnoe bei pulmonaler Metastasierung). In ca. zwei Drittel der Fälle findet sich eine pathologische vaginale Blutung. Im Gegensatz zu Karzinomen sind die Hysteroskopie und Abrasio nicht immer diagnostisch beweisend. So kann das Ergebnis bei mesenchymalen Tumoren des Uterus nicht selten falsch negativ sein, das heißt, letztere bleiben häufig zunächst unentdeckt, wenn sich bei Blutungsstörungen oder Postmenopausenblutungen die Indikation zur histologischen Abklärung ergibt.
Bei klinischem Verdacht auf ein Malignom des Uterus sind sogenannte morcellierende Verfahren (zerstückeln) kontraindiziert, da diese zu einer Prognoseverschlechterung führen [2]. In jedem Falle soll bei geplantem Morcellement auch bei klinisch nicht suspekt erscheinendem Tumor die Patientin über das Risiko der möglichen Tumorzellverschleppung aufgeklärt und alternative Verfahren angeboten werden.
Bezüglich bildgebender Diagnostik von uterinen Sarkomen stellt die transvaginale Sonografie derzeit das primäre diagnostische Verfahren zur Beurteilung des Uterus dar. Weiterhin zu empfehlen ist der Einsatz der MRT zur lokalen Ausbreitung und zur Erfassung der lokalen Tumorinfiltration.
Aufgrund des hohen Metastasierungspoten-zials sollte eine Computertomografie des Abdomens und des Thorax erfolgen.
In jedem Fall sollte die Patientin mit der Diagnose eines uterinen Sarkoms in einer interdisziplinären Tumorkonferenz vorgestellt werden.
Uterine Karzinosarkome/Maligne Müllersche Mischtumoren
Die Prognose dieser Tumore ist generell eingeschränkt. So beträgt die Fünf-Jahres-Überlebensrate im Stadium I/II ca. 50 bis 60 Prozent, und fällt in fortgeschrittenen Stadien signifikant ab (Stadium III/IV – ca. zehn bis 20 Prozent).
Im Frühstadium ist die Entfernung des Uterus und beider Adnexe in toto der Goldstandard des operativen Managements (Konsensusstärke +++). In Analogie zum Hoch-Risiko-Endometriumkarzinom gibt es retrospektive Datenanalysen, welche einen positiven Einfluss einer systematischen Lymphadenektomie auf das Gesamtüberleben der Patientinnen beschreiben, wobei ein positiver Lymphknotenstatus bei makroskopisch auf den Uterus begrenzter Erkrankung in bis zu 30 Prozent auftreten kann [3].
Im fortgeschritten Stadium kann eine zyto-reduktive Operation durchgeführt werden, wenn eine Komplettresektion erreichbar scheint, wobei die Datenlage diesbezüglich limitiert ist.
Aufgrund der ungünstigen Prognose ist bei diesen Patientinnen postoperativ adjuvant sowohl eine Systemtherapie, als auch eine lokoregionäre Bestrahlung zu diskutieren.
In einer randomisierten Phase-III-Studie an insgesamt 232 Patientinnen mit Karzinosarkomen konnte durch eine adjuvante (ergänzend zur OP) Kombinations-Chemotherapie mit Cisplatin/Ifosfamid im Vergleich zu einer Ganz-Abdomenbestrahlung bei FIGO-Stadium I bis IV und einem postoperativen Tumorrest von < 1 cm das Risiko, im Nachbeobachtungszeitraum von fünf Jahren zu versterben, um 29 Prozent – jedoch nicht signifikant – reduziert werden [4]. Darüber hinaus existieren Daten aus retrospektiven Analysen, welche einen positiven Effekt einer solchen Therapie auch in frühen Stadien (I und II) vermuten lassen [5].
Die Entscheidung zur adjuvanten Chemotherapie muss mit der Patientin individuell unter Berücksichtigung des Befundes und nach ausführlicher Aufklärung über die Nebenwirkungen besprochen werden.
Eine adjuvante Beckenbestrahlung per externer Teletherapie mit 50,4 Gy im Stadium I oder II zeigte in einer randomisierten Studie [6] speziell für die Subgruppe der Patientinnen mit Karzinosarkom (n=92) eine verbesserte lokale Kontrolle mit einer Reduktion der Lokalrezidivrate von 47 Prozent auf 24 Prozent im Beobachtungszeitraum (mediane Nachbeobachtung 6,8 Jahre).
Aufgrund der Verbesserung der lokalen Kontrolle sollte daher beim Karzinosarkom die Indikation zu einer postoperativen Radiotherapie bei Stadium FIGO I/II gestellt werden.
Im Fall einer bereits metastasierten Erkrankung ist eine palliative Systemtherapie in Erwägung zu ziehen.
Mono-Chemotherapie-Schemata sind beim Karzinosarkom aufgrund unzureichender Therapieeffekte weder in der adjuvanten- noch in der metastasierten Situation in größeren Phase-II- oder Phase-III-Studien untersucht worden. Akzeptable Ansprechraten bis 36 Prozent liegen nur zur Ifosfamid-Monotherapie vor [7]. Bezüglich Kombinations-Therapien ergab die jüngste Cochrane-Analyse ein signifikant reduziertes Risiko zu versterben bei Gabe einer Ifosfamid-Kombination im Vergleich zu einer Ifosfamid Monotherapie (HR Tod 0,75, CI 0,6 bis 0,94) [8]. Aus dieser Analyse konnte im Rahmen einer Phase-III-Studie [9] ein signifikanter Vorteil der Kombination von Ifosfamid und Paclitaxel im Vergleich zu Ifosfamid allein sowohl für das progressionsfreie als auch das Gesamtüberleben demonstriert werden, sodass dieses Schema als mögliche Kombination empfohlen werden kann. Weitere wirksame Kombinationen sind Carboplatin und Paclitaxel sowie Carboplatin und pegyliertes liposomales Doxorubicin.
Uterine Leiomyosarkome (LMS)
Leiomyosarkome sind sehr aggressive Tumoren und mit einer ungünstigen Prognose assoziiert, selbst dann, wenn der Tumor noch auf den Uterus begrenzt ist. Die Rezidivraten schwanken zwischen 53 und 71 Prozent. In einer Untersuchung aus Norwegen betrug die Fünf-Jahres-Überlebensrate auch im Stadium I nur 51 Prozent und im Stadium II 25 Prozent [10].
Die Entfernung des Uterus in toto ist der Goldstandard des operativen Managements. (Konsens +++) Die Indikation zur Adnexexstirpation ist fakultativ in Abhängigkeit vom Menopausenstatus zu stellen. Bei jungen Frauen mit auf den Uterus beschränkten Tumoren können die Ovarien erhalten werden [3, 11].
Die Inzidenz von primären pelvinen und para-aortalen Lymphknotenmetastasen ist beim LMS niedrig. Sind die Lymphknoten – hierbei häufig bereits intraoperativ auffällig – befallen, liegt meist auch schon eine hämatogene Metastasierung vor. Insofern ist eine systematische pelvine und paraaortale Lymphadenektomie nicht mit einer verbesserten Prognose verbunden und wird im Allgemeinen nicht empfohlen. Suspekte Lymphknoten sollten dennoch entfernt werden.
Bei ausgedehnten, fortgeschrittenen Befunden und Symptomatik sollte ebenso der Versuch der operativen Tumorreduktion erfolgen [11].
Eine adjuvante systemische Therapie ist nicht generell indiziert, da bislang in keiner randomisierten Studie ein Vorteil im Gesamtüberleben nachgewiesen werden konnte. Aus den bisher vorliegenden Ergebnissen scheinen Patientinnen mit Leiomyosarkom, bei denen der Tumor auf den Uterus begrenzt ist eventuell von einer systemischen Therapie nach Operation ohne Resttumor zu profitieren.
Eine Kombination aus Doxorubicin/Ifosfamid/Cisplatin hat einen signifikanten positiven Effekt auf das Drei-Jahres-progressionsfreie Überleben (55 Prozent mit folgender Radiotherapie gegenüber 41 Prozent in der Kontrollgruppe mit alleiniger Radiotherapie) zu haben, jedoch einhergehend mit einer deutlich höheren Toxizität [12].
Ähnlich gute Ergebnisse mit jedoch geringerer Toxizität ergibt sich für eine Kombinations-Chemotherapie mit Docetaxel und Gemcitabine gefolgt von Doxorubicin (3-Jahre PFS 57 Prozent) [13].
Die adjuvante Beckenbestrahlung mit 50,4 Gy im Stadium I oder II zeigte [6] zwar eine verbesserte lokale Kontrolle für das Gesamtkollektiv der unterschiedlichen Sarkomentitäten, jedoch in der Subgruppe der Patientinnen mit Leiomyosarkomen (n=99) keinen Effekt auf die Lokalrezidivrate (20 Prozent mit Strahlentherapie – 24 Prozent ohne Strahlentherapie). Somit ist eine Strahlentherapie bei Komplettresektion eines LMS im Stadium I/II im Allgemeinen nicht indiziert.
Bei Rezidiven bzw. Metastasen uteriner Leiomyosarkome scheint die operative Komplettresektion mit einer verbesserten Prognose assoziiert zu sein [14]. Es sollte deshalb bei jedem Rezidiv bzw. isolierten Metastasen geprüft werden, inwieweit eine Komplettresektion möglich und sinnvoll ist. Ein krankheitsfreies Intervall von mehr als sechs bis zwölf Monaten bei Leiomyosarkomen zeigte ein verbessertes Überleben nach Metastasenresektion, wohingegen ein verkürztes erkrankungsfreies Intervall als auch eine inkomplette Resektion mit einer schlechteren Prognose assoziiert war.
Die Überlegenheit einer Kombinations- über eine Mono-Chemotherapie in dieser Situation ist bisher nur für die Kombination Docetaxel/Gemcitabine gezeigt worden [15].
Einige Kombinationen zeigen höhere Ansprechraten als Mono-Chemotherapien in der Metastasierung, allerdings einhergehend mit einer höheren Toxizität.
Für die Mono-Chemotherapie gibt es nur wenige wirksame Substanzen, wie zum Beispiel Ifosfamid, oder Doxorubicin mit moderaten Ansprechraten zwischen 15 und 25 Prozent.
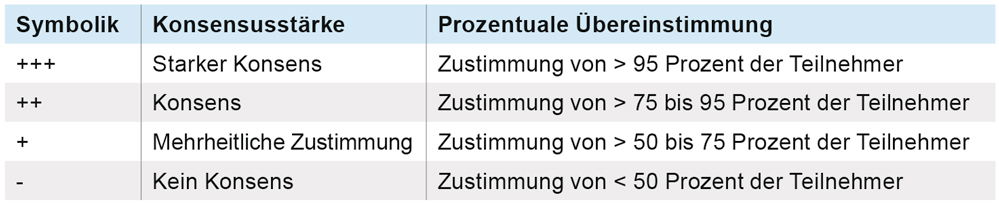
Tabelle 2: Einteilung zur Zustimmung der Konsensusbildung.
Low-grade Endometriale Stromasarkome (LG-ESS)
Das LG-ESS hat tendenziell eine eher günstige Prognose. Die Rate für das krankheitsspezifische Fünf-Jahres-Überleben beträgt 80 bis 90 Prozent, für das Zehn-Jahres-Überleben ca. 70 Prozent [16]. Ist der Tumor zum Zeitpunkt der Diagnose auf den Uterus begrenzt (Stadium I) betragen die Raten sogar 100 Prozent bzw. 90 Prozent. In höheren Stadien fällt die Rate auf bis zu 40 Prozent.Die Therapie der Wahl ist die totale Hysterektomie mit Entfernung beider Adnexe (Konsens +++) [17].Die Therapie der Wahl ist die totale Hysterektomie mit Entfernung beider Adnexe (Konsens +++) [17].Die Therapie der Wahl ist die totale Hysterektomie mit Entfernung beider Adnexe (Konsens +++) [17].
Die endokrine Abhängigkeit des LG-ESS ist gut belegt. So zeigt eine retrospektive Analyse von 153 LG-ESS Patientinnen eine signifikant erhöhte Rezidivrate bei Belassen der Ovarien bei prämenopausalen Patientinnen. Sowohl in dieser Analyse als auch in zwei weiteren Auswertungen der SEER-Datenbank ergab sich allerdings kein negativer Einfluss auf das Gesamtüberleben. Insofern sollten die Vorteile eines Ovarerhaltes bei jungen Patientinnen gegenüber dem Risiko einer höheren Rezidiv-wahrscheinlichkeit sorgfältig abgewogen und mit den Patientinnen kritisch diskutiert werden [18, 19].
Es gibt keine Daten zur onkologischen Sicherheit des Einsatzes einer Hormonersatztherapie nach durchgeführter Primärbehandlung eines LG-ESS. Von daher sollte aufgrund der Tumorbiologie von einer solchen Therapie abgeraten werden.
Ein Lymphknotenbefall scheint keinen Einfluss auf die Prognose zu haben. Insofern ist von einer systematischen Lymphadenektomie, als auch von darauf aufbauenden adjuvanten Therapieoptionen kein verlängertes Überleben zu erwarten, sodass die Lymphadenektomie insgesamt nicht als Standard empfohlen werden kann.
Ob bei fortgeschrittenen Tumoren eine Zytoreduktion einen Einfluss auf das Überleben der Patientinnen hat ist unklar. Die Indikation hierzu ergibt sich – gegebenenfalls in palliativer Intention – aus dem klinischen Beschwerdebild der Patientin.
Eine postoperative adjuvante endokrine Therapie kann mit der Patientin ab Stadium FIGO III diskutiert werden, obwohl prospektive Studien dazu fehlen. Die Daten zur adjuvanten Therapie sprechen für den Einsatz von entweder Medroxyprogesteronacetat 200 mg/die (in Deutschland lediglich als 250 mg Dosis erhältlich) bzw. Megestrolacetat 160 mg/die oder alternativ für einen Aromatasehemmer (Letrozol 2,5 mg/die, Anastrozol 1 mg/die oder Exemestan 25 mg/die). Die adjuvante Therapiedauer ist unzureichend untersucht. Es wird eine Zeitdauer von fünf Jahren diskutiert.
Für eine adjuvante Chemotherapie liegen keine validen Daten vor.
Eine große epidemiologische Studie aus den USA an 3.650 Patientinnen mit Uterussarkomen ergab sowohl einen signifikant positiven Einfluss einer adjuvanten Beckenbestrahlung (± Brachytherapie) auf das lokoregionär-rezidivfreie Überleben im gesamten Kollektiv [20], als auch in der Subgruppe der Patientinnen mit ESS (Endometriales Stromasarkom) (n=361: nach fünf Jahren 97 Prozent gegenüber 93 Prozent bzw. nach acht Jahren 97 Prozent gegenüber 87 Prozent). Eine weitere große epidemiologische Studie aus den USA an insgesamt 1.010 Patientinnen mit ESS konnte jedoch bezüglich des Gesamtüberlebens keinen signifikanten Benefit einer adjuvanten Strahlentherapie nachweisen [16]. Somit scheint beim endometrialen Stromasarkom die postoperative Strahlentherapie lediglich eine mäßiggradige weitere Verbesserung der ohnehin guten lokoregionären Kontrolle zu ermöglichen, was deshalb gegen die mittel- und langfristigen Nebenwirkungen abzuwägen ist.
Bei jedem Rezidiv bzw. Metastasen sollte überprüft werden, ob eine Operation mit dem Ziel der makroskopischen Komplettresektion möglich ist. Aufgrund ihres langsamen Wachstums können gegebenenfalls auch wiederholte Resektionen bei LG-ESS einen Benefit mit sich bringen.
Bei postoperativem Residualtumor, inoperablen Rezidiven oder Fernmetastasen von LG-ESS kann eine Systemtherapie zum Einsatz kommen. Aufgrund ihrer hohen Expression von Östrogen- und Progesteronrezeptoren kommen hierbei Gestagene zum Einsatz [21, 22]. Es sind Ansprechraten bis 82 Prozent beschrieben [21]. Obwohl weniger Daten vorliegen, scheinen alternativ auch Aromatasehemmer (Letrozol 2,5 mg/die, Anastrozol 1 mg/die oder Exemestan 25 mg/die) einen positiven Effekt zu haben [22].
Eine Chemotherapie sollte nur eingesetzt werden, wenn andere Optionen erschöpft sind.
High-grade endometriale Stromasarkome und undifferenzierte uterine Sarkome (HG-ESS; UUS)
Aufgrund der häufigen Detektion in fortgeschrittenen Stadien ist die Prognose mit einem medianen Gesamtüberleben von ein bis zwei Jahren sehr ungünstig [23].
Die Therapie der Wahl besteht aus einer totalen Hysterektomie und einer Adnexexstirpation beidseitig. Ob die Adnexe in der Prämenopause belassen werden können ist unklar. Zwar sind positive pelvine und/oder para-aortale Lymphknoten mit einer schlechteren Prognose assoziiert, allerdings gibt es keinen Hinweis darauf, dass durch die operative Entfernung und darauf aufbauende adjuvante Therapieoptionen diese eingeschränkte Prognose verbessert wird.
Ob bei fortgeschrittenen Tumoren eine Zytoreduktion einen Einfluss auf das Überleben der Patientinnen hat, ist unklar. Eine multizentrische retrospektive Analyse konnte jedoch diesbezüglich – im Gegensatz zu den LG-ESS – einen positiven Effekt einer Zytoreduktion auf das Überleben nachweisen.
Eine postoperativ adjuvante endokrine Therapie kann in Analogie zum LG-ESS mit der Patientin dann besprochen werden, wenn im Tumor Estrogen- und/oder Progesteronrezeptoren nachgewiesen sind, obwohl auch hier prospektive Studien fehlen.
Bei ungünstiger Prognose dieses histologischen Typs und fehlenden Alternativen in der adjuvanten Therapie kann die Nutzen-Risiko-Bewertung bei der Aufklärung der Patientin für den Einsatz von Medroxyprogesteronacetat 200 mg/die (in Deutschland lediglich als 250 mg Dosis erhältlich) oder Megestrolacetat 160 mg/die sprechen. Alternativ ist hier ebenso ein Aromatasehemmer (Letrozol 2,5 mg/die, Anastrozol 1 mg/die oder Exemestan 25 mg/die) in Betracht zu ziehen. Die adjuvante Therapiedauer ist unzureichend untersucht.
Für eine adjuvante Chemotherapie liegen keine validen Daten vor, sodass dies individuell besprochen werden sollte.
In einer multizentrischen retrospektiven Analyse wurden 59 Patientinnen mit endometrialen Stromatumoren untersucht, davon n=29 mit undifferenziertem uterinen Sarkom [24]. 86 Prozent der Patientinnen erhielten eine externe Teletherapie des Beckens bzw. 51 Prozent eine Brachytherapie. Für die Patientinnen mit undifferenziertem uterinen Sarkom betrug nach fünf Jahren das Gesamtüberleben 65 Prozent, die lokoregionäre Kontrolle 40 Prozent. Die Beckenbestrahlung war in der Gesamtgruppe (endometriales Stromasarkom und undifferenziertes uterines Sarkom) in multivariater Analyse mit einem signifikant verbesserten Gesamtüberleben assoziiert. Somit besteht beim undifferenzierten uterinen Sarkom eine limitierte Datenlage zur Radiotherapie.
Im Falle einer disseminierten Metastasierung kann – obwohl nur wenige Daten vorliegen – in Analogie zum LG-ESS eine endokrine Therapie mit der Patientin dann besprochen werden, wenn im Tumor Estrogen- oder Progesteronrezeptoren nachgewiesen werden.
Darüber hinaus besteht die Option einer Chemotherapie in Analogie zu anderen Weichteilsarkomen (zum Beispiel Leiomyosarkom), wobei die Daten hierfür insgesamt ebenso limitiert sind.
Nachsorge
Die Nachsorge dient primär der Sicherung des Heilerfolges und der Lebensqualität.
Die tumorspezifisch orientierte Nachsorge der Patientin mit Spekulumeinstellung, vaginaler und rektaler Untersuchung und gegebenenfalls Ultraschall sollte in regelmäßigen Abständen erfolgen.
Ob eine lokale Intervention bei frühzeitig detektiertem uni-lokulärem Rezidiv zu einer Verbesserung des Gesamtüberlebens führt ist unklar.
Gleichwohl kann eine weiterführende bildgebende Diagnostik zur Früherkennung von Metastasen sinnvoll sein.
Das Literaturverzeichnis kann im Internet unter www.bayerisches-ärzteblatt.de (Aktuelles Heft) abgerufen werden.
Die Autoren erklären, dass sie keine finanziellen oder persönlichen Beziehungen zu Dritten haben, deren Interessen vom Manuskript positiv oder negativ betroffen sein könnten.

Professor Dr. Matthias W. Beckmann

Professor Dr. Dominik Denschlag
Teilen:
Das könnte Sie auch interessieren: