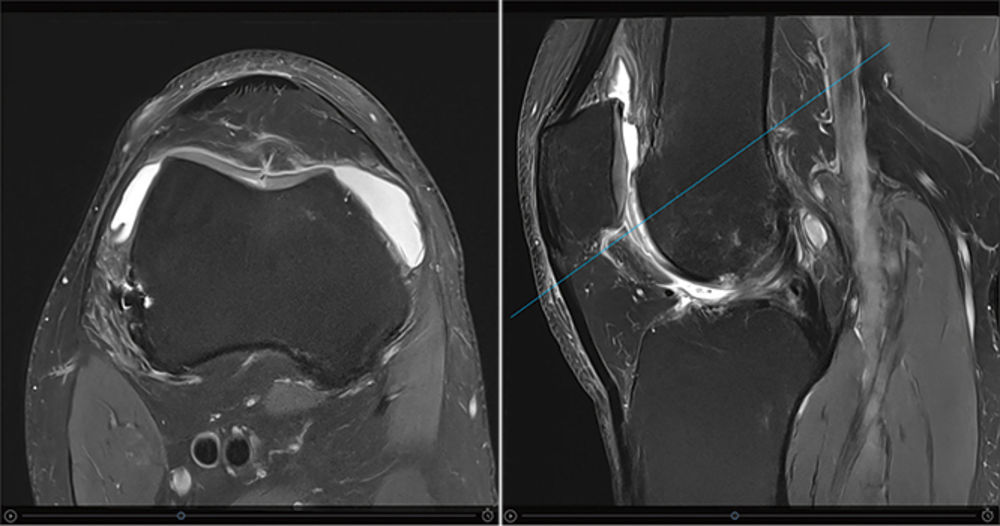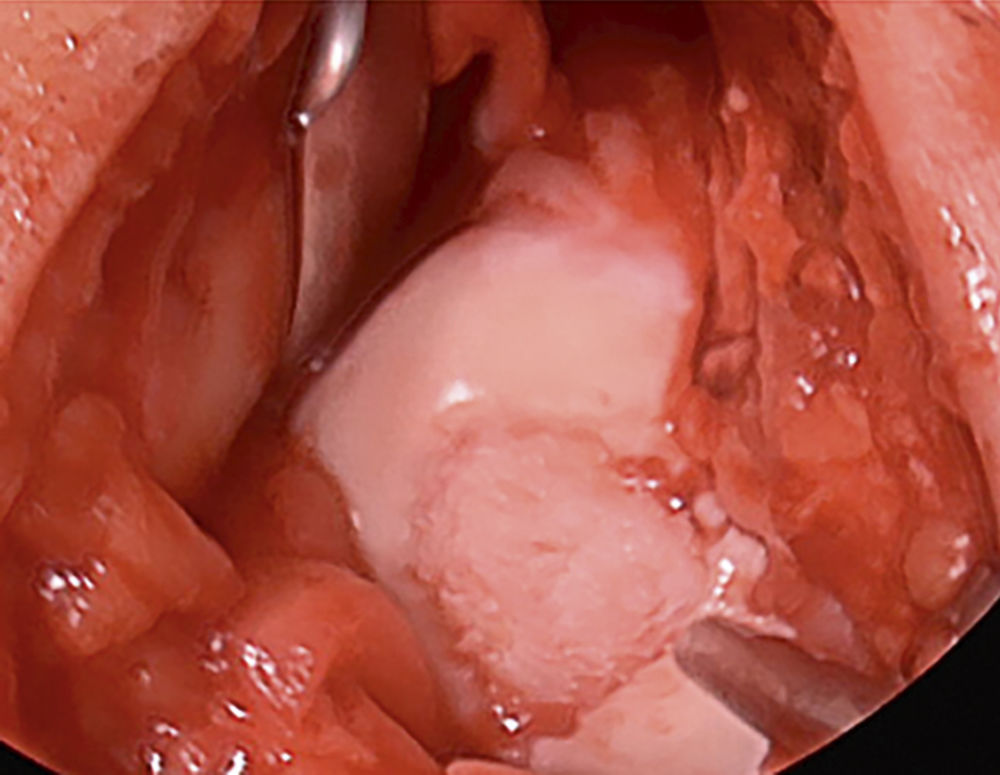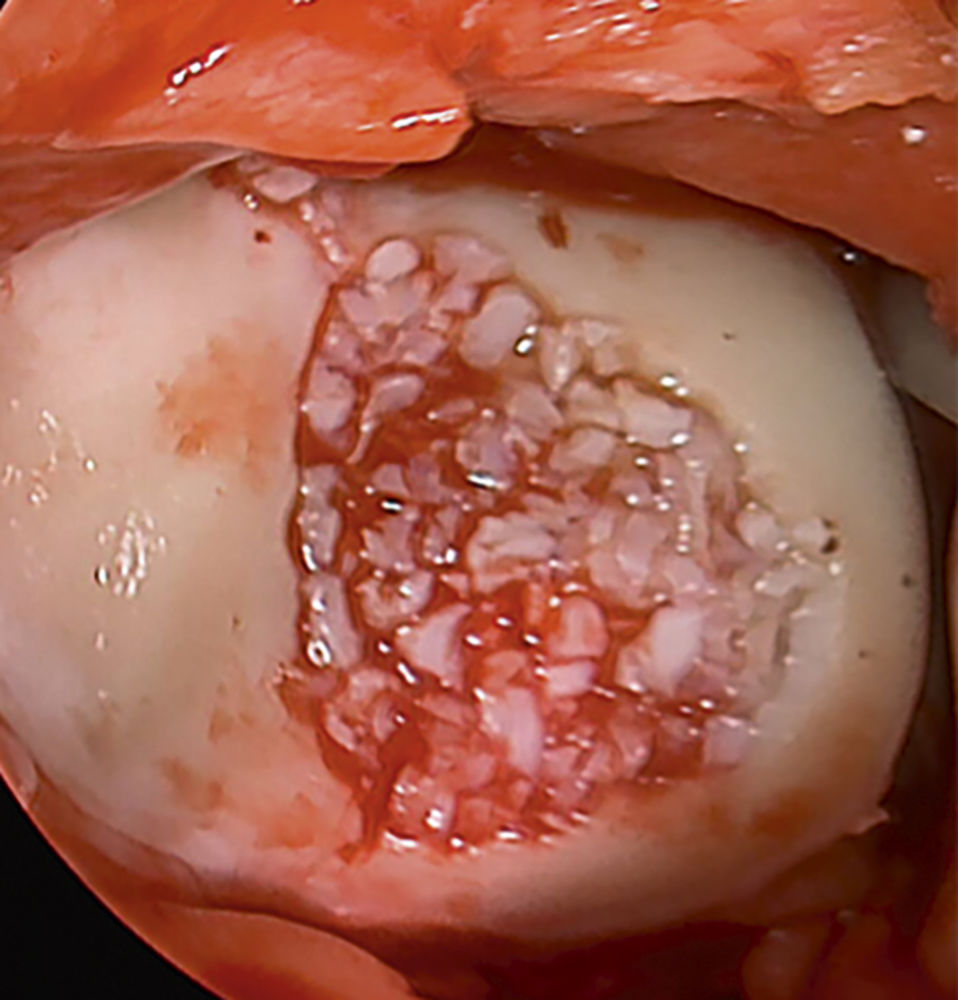
Abbildung 3, 4: Knorpeldefekt debridiert und mit Knorpelzellfragmenten gefüllt.
Vergleichende Studien konnten für die autologe Knorpeltransplantation (ACT) bei Arthrose im Vergleich zur einfachen Kniegelenkslavage, subchondrale Bohrungen nach Pridie oder Mikrofrakturierung (hierbei wird iatrogen ein kleiner Knorpeldefekt gesetzt um im Gelenk einen Reparaturmechanismus auszulösen) eine deutlich bessere Defektfüllung zeigen [1].
Die Methodik der Matrixgestützten Autologen Chondrozytentransplantation (M-ACT) hat sich in den vergangenen Jahren als Standardverfahren für Knorpelzelldefekte > 2 cm2 etabliert. Bei diesem Verfahren wird die Matrix im externen Labor aus Knorpelzellen des Patienten hergestellt und in einem zweizeitigen Operationsverfahren reimplantiert. Das Verfahren ist kostenintensiv und benötigt zwei Operationen [2].
Eine Studie aus dem Jahr 2024 zeigt als neue Behandlungsalternative, dass die „Minced Cartilage“-Technik als einzeitiges Verfahren wirksam ist und die klinischen und radiologischen Ergebnisse mindestens vergleichbar zu alternativen operativen Techniken waren [3].
Das Nachbehandlungsschema empfiehlt eine sechs Wochen andauernde Teilbelastung. Eine gerade Knieschiene mit einer Beugestellung von 0° sollte ohne Bewegungsübungen für 48 Stunden bis zu einer Woche, je nach Defektgröße, getragen werden. Danach erfolgt die Anpassung einer Orthese mit Flexions- und Extensionsbeschränkung und passive Bewegung in einer motorbetriebenen Bewegungsschiene. Zwischen der 2. und 6. postoperativen Woche sollte die passive Flexion von 30° auf 90° gesteigert werden. Nach sechs Wochen kann eine schmerzadaptierte Vollbelastung bei freier Beweglichkeit begonnen werden. Nach einem Jahr sollte eine MRT-Untersuchung wiederholt werden um den Erfolg der Therapie zu kontrollieren.
Fall 2: Individualisierte Endoprothetik
Ein 65-jähriger Patient klagt über Schmerzen im Bereich seines linken Kniegelenkes. Die Schmerzen projizieren sich insbesondere auf die Innenseite des Kniegelenkes und treten in Belastungssituationen sowie zunehmend auch in Ruhe auf. Der Patient wünscht eine nachhaltige Verbesserung seiner Lebensqualität, um insbesondere auch moderate sportliche Aktivitäten wieder aufnehmen zu können.
Die Untersuchung ergibt eine mild varische Beinachse, einen provozierbaren Schmerz über dem medialen Kniegelenk bei gut erhaltener Beweglichkeit mit einer Flexion von 140° bei nahezu voller Streckfähigkeit und einem in allen Ebenen bandstabilen Gelenk. In den radiologischen Aufnahmen zeigt sich eine isolierte anteromediale Arthrose mit intaktem lateralen Gelenkkompartiment (Abbildung 5 bis 7).
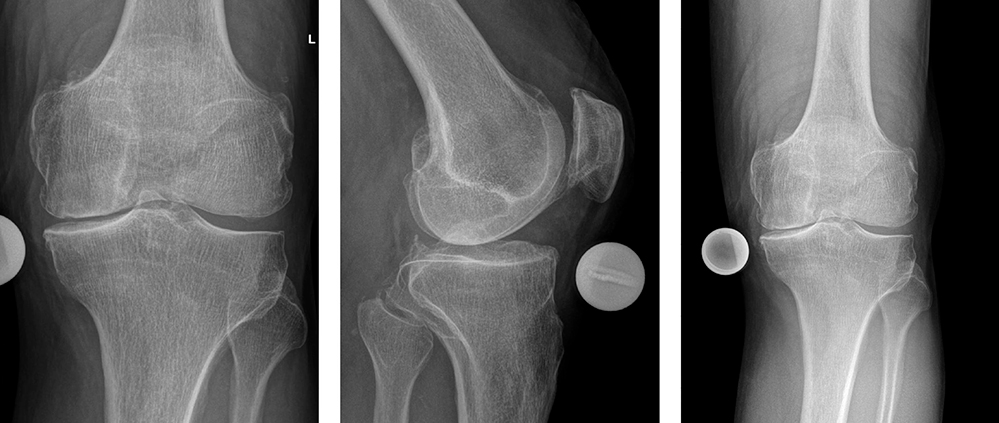
Abbildung 5 bis 7: Röntgenbilder des Kniegelenkes in zwei Ebenen und belastete Ganzbeinstandaufnahme mit der Darstellung
einer medialen Gonarthrose bei varischer Beinachse.
Das mitgeführte MRT des Kniegelenkes bestätigt die Diagnose, stellt jedoch eine in der Regel nicht notwendige Untersuchung dar (Abbildung 8 bis 10).
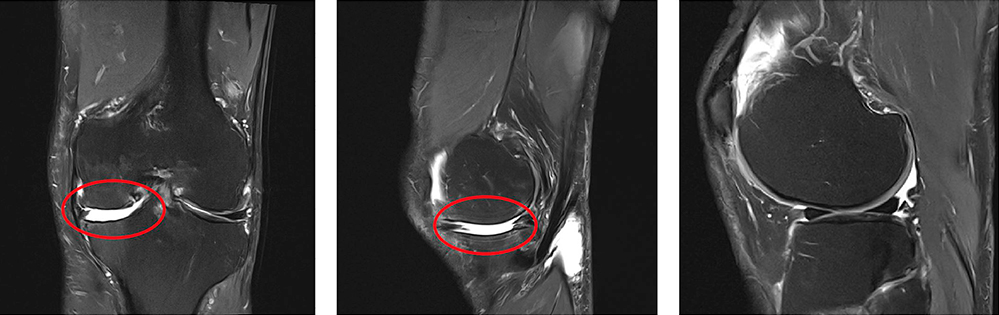
Abbildung 8 bis 10: Sagittale und frontale MRT-Schichten des Kniegelenkes mit Darstellung eines vollschichtigen flächigen
Knorpelschadens medial femoral distal und tibial anterior, wohingegen der Knorpel dorsal femoral und auch tibial erhalten ist.
Es liegt eine Streckspaltarthrose medial bei komplett erhaltenem Knorpel und Meniskus im lateralen Kompartiment vor.
Im folgenden Beratungsgespräch werden die therapeutischen Optionen mit dem Patienten besprochen. Ein möglicher konservativer Therapieansatz beruht auf mehreren Säulen. Es kommt eine analgetische Therapie mit zum Beispiel NSAR zum Einsatz, aktivierende und bewegungserhaltende Maßnahmen, eine Anpassung des Körpergewichts und gegebenenfalls Injektionen mit Corticosteroiden, Hyaluronsäure oder auch angereichertem Plasma [6].
Im aktuellen Fall war bereits eine orale analgestische Behandlung mit einem NSAR, eine physiotherapeutische Übungsbehandlung und mehrfache intraartikuläre Injektionen mit Hyaluronsäure erfolgt und der Patient wünscht explizit die operative Therapie. Bei der Diagnose einer isolierten medialen Gonarthrose geben die aktuellen Leitlinien der Gesellschaft für Orthopädie und Unfallchirurgie die Empfehlung, die unikondyläre Endoprothese gegenüber der Totalendoprothese abzuwägen.
Während sowohl in Landesregistern als auch Studien die klinischen und funktionellen Ergebnisse der unikondylären Teilendoprothesen den Totalendoprothesen überlegen sind, zeigen sich die mittel- und langfristigen Standzeiten der Teilendoprothesen denen der Totalendoprothesen unterlegen [7, 8].
Gründe für diese geringere Langlebigkeit sind eine inkorrekte Indikationsstellung, die anspruchsvolle Operationstechnik, die Häufigkeit der Anwendung des Operateurs sowie Implantateigenschaften [7]. Hier könnte sich eine aktuelle Entwicklung als wegweisende Verbesserung ergeben. Um die operative Präzision zu steigern und den Eingriff zu vereinfachen, stellen robotische Assistenzsysteme einen vielversprechenden Ansatz dar. Der positive Einfluss auf die Präzision der Operation konnte bereits mehrfach nachgewiesen werden [9]. Unterschieden werden bildlose, durch intraoperative Navigationsdaten unterstützte robotische Assistenten, und bildbasierte Systeme, welche eine präoperative ausgeweitete Bildgebung, wie zum Beispiel ein CT, voraussetzen [10]. Durch das Aufzeichnen der patienteneigenen spezifischen Anatomie und Erfassung der Bandspannung ist eine Echtzeit-Simulation des operativen Eingriffs, abhängig von der gewählten Implantatposition, möglich (Abbildung 11, 12). Auf diesem Weg kann sowohl das klinische Ergebnis als auch die Standzeit positiv beeinflusst werden. Mittelfristige Ergebnisse aus dem australischen Endoprothesenregister konnten bereits eine signifikante Verbesserung der Langlebigkeit unikondylärer Prothesen zeigen [11].
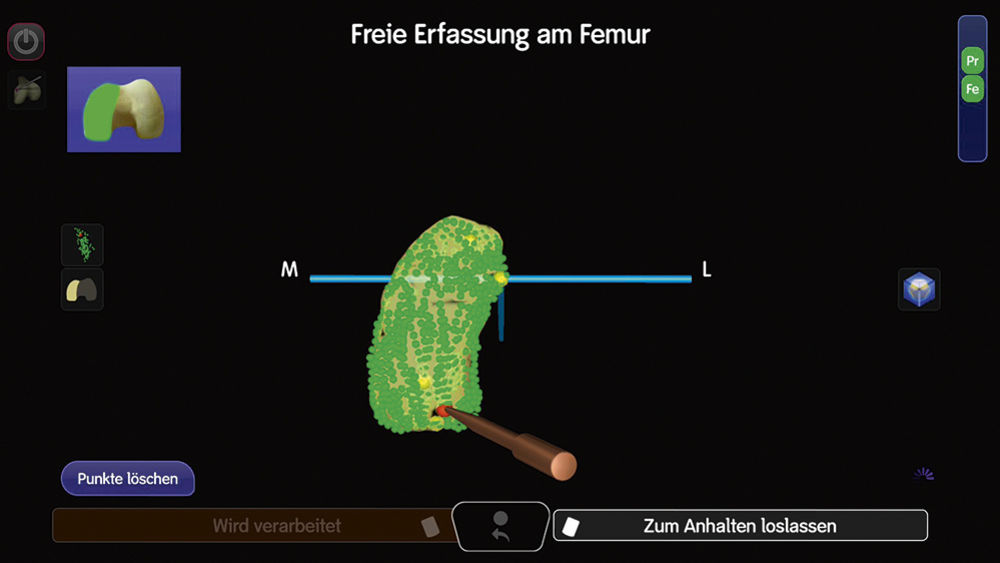
Abbildung 11: Darstellung der Sammlung der individuellen Anatomie, beispielhaft des Femurs, des Patienten. Die Oberfläche wird durch eine Vielzahl von Punkten mithilfe der Navigation aufgenommen und rekonstruiert.
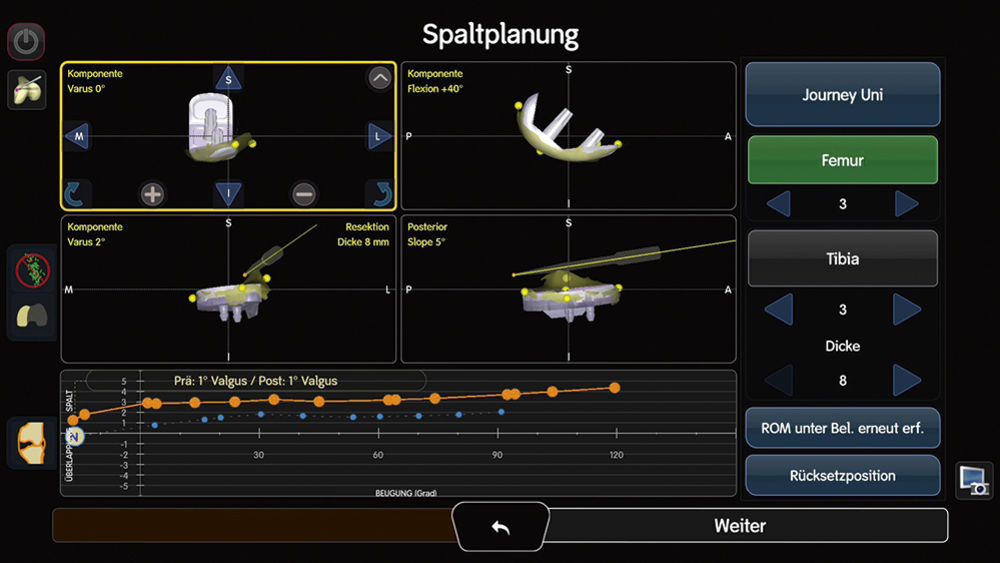
Abbildung 12: Beispiel einer Simulation der Implantatpositionierung an Femur und Tibia und die Auswirkung auf die zu erwartende
Funktionalität des Gelenkes. Es kann zudem eine möglichst optimale knöcherne Abdeckung erreicht werden, um die Fixation des Implantates zu optimieren.
Nach einem informativen Aufklärungsgespräch wurde im vorliegenden Fall gemeinsam entschieden, eine mediale Teilprothetik durchzuführen, um einen möglichst hohen Gewinn an Lebensqualität zu ermöglichen (Abbildung 13, 14).
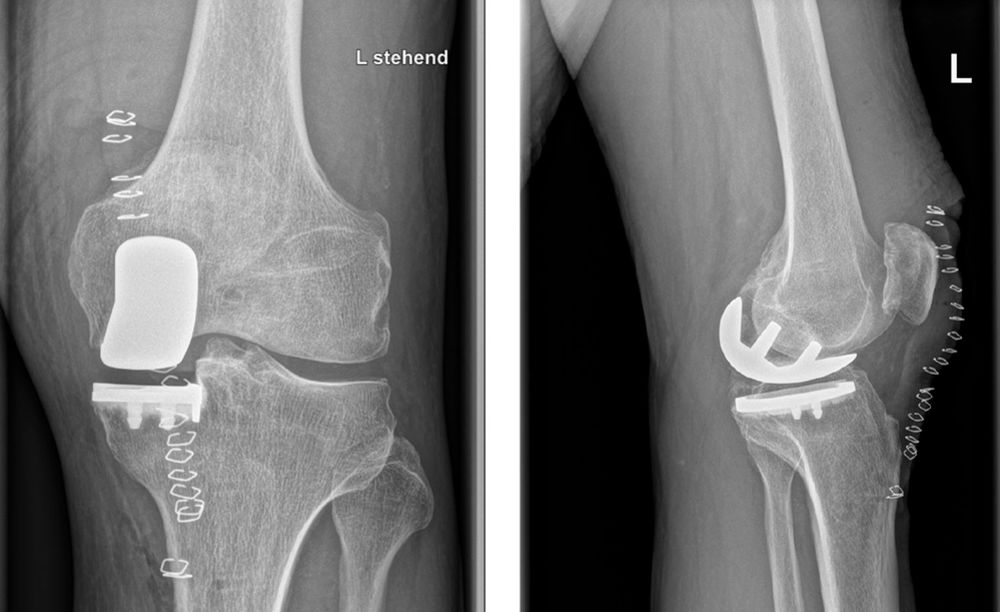
Abbildung 13, 14: Postoperative Röntgenbilder in zwei Ebenen nach Roboter-assistierter medialer Schlittenprothesen-Implantation.
Fall 3: 3D-Planung und patientenspezifische Instrumente in der Schulterendoprothetik
Ein 70-jähriger Patient wurde mit zunehmenden rechtsseitigen Schulterschmerzen und erheblichen Bewegungseinschränkungen in unsereSchultersprechstunde überwiesen. Vor zehn Jahren wurde erstmals eine transmurale Supraspinatussehnenruptur diagnostiziert, die bei kompensiertem Schmerz und guter Funktion erfolgreich konservativ behandelt worden war. In den vergangenen zwei Jahren dekompensierten Funktion und Schmerzsituation zunehmend. Ein MRT zeigte eine Progredienz der Rotatorenmanschettenruptur mit fortgeschrittener Sehnenretraktion, Muskelatrophie und Ruptur der kompletten Infraspinatussehne. Ferner hatte sich aufgrund der insuffizienten Gelenkzentrierung eine Defektarthropathie mit exzentrischem Abrieb des Glenoids entwickelt. In der klinischen Untersuchung waren aktive Abduktion und Elevation im Schultergelenk auf 60° begrenzt, die Außenrotation war bis 10° möglich. Passiv war das Gelenk frei beweglich. Der Patient klagte über persistente Nacht- und Ruheschmerzen, die unter ausgedehnter konservativer Therapie nicht mehr beherrschbar waren, sodass wir uns nach entsprechendem Aufklärungsgespräch für die Implantation einer inversen Schulterprothese entschieden haben.
Der exzentrische Glenoiddefekt stellt in diesen Situationen eine Herausforderung dar, denn trotz der Fortschritte beim Implantatdesign und bei der Operationstechnik sind fehlimplantierte Glenoidkomponenten mit Lockerungen und Instabilitäten eine der Hauptursachen für das langfristige Versagen von Schulterprothesen [12]. Eine präoperative 3D-Planung hilft die Präzision der Platzierung der Glenoidkomponenten im Vergleich zur konventionellen 2D-Planung signifikant zu verbessern [13]. Als Grundlage für eine 3D-Rekonstruktion dient ein hochauflösender CT-Scan der Schulter mit gesamter Skapula. Die CT-Daten werden dann in eine spezielle Planungssoftware übertragen. Anhand dieser Daten wird ein virtuelles 3D-Modell des Schultergelenks erstellt und der Operateur kann verschiedene Prothesentypen und -größen virtuell testen, um die beste Passform zu ermitteln (Abbildung 15).
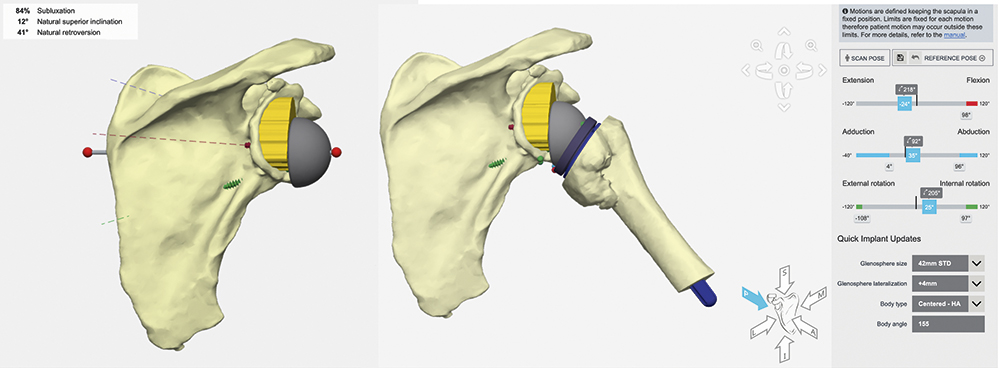
Abbildung 15: 3D-Planung und virtuelle Bewegungsanalyse einer inversen Schulterprothese mit Knochentransplantat (gelb) zur Korrektur einer schweren Glenoiddeformität.
Falls nötig, können Knochentransplantationen oder Spezialkomponenten zur Defektrekonstruktion eingeplant werden. Abschließend kann der Bewegungsumfang virtuell simuliert und mit verschiedenen Planungsvarianten verglichen werden, um das bestmögliche Ergebnis für die individuelle Anatomie zu ermitteln.
Insbesondere bei komplexen Deformitäten können patientenspezifische Instrumente die Platzierung von Glenoidkomponenten sowohl in der Version als auch in der Neigungsebene im Vergleich zur Standardinstrumentierung noch weiter verbessern [14, 15]. Basierend auf der 3D-Planung werden innerhalb weniger Tage spezielle Bohrschablonen aus Kunststoff entworfen, die auf die individuelle Anatomie des Patienten zugeschnitten sind (Abbildung 16).
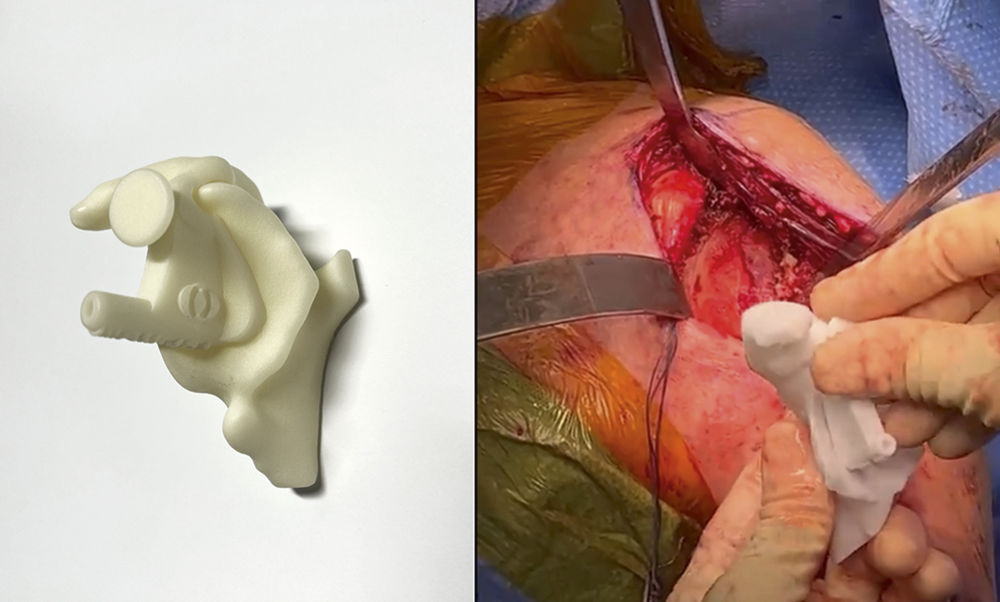
Abbildung 16: Patientenspezische Instrumentierung (PSI) der Schultergelenkspfanne mit Zielvorrichtung und Glenoidschablone.
Diese individuellen Zielvorrichtungen dienen als Führungshilfe während der OP, um die zuvor geplante Positionierung der Prothese exakt umzusetzen. Die 3D-Modelle der Schultergelenkspfanne können außerdem als Vorlage zur Anpassung eines autologen Knochentransplantats verwendet werden, das in den meisten Fällen aus dem resezierten Humeruskopf gewonnen wird (Abbildung 17).
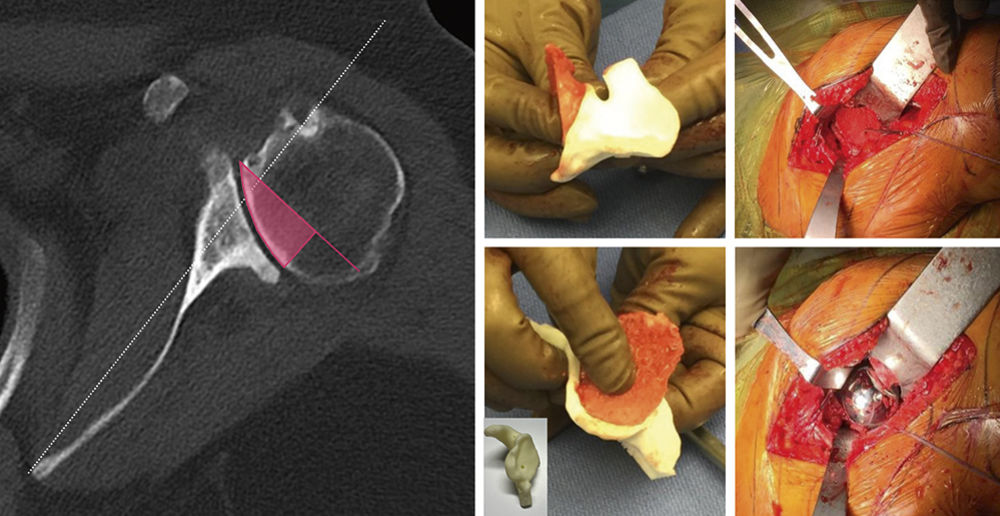
Abbildung 17: 3D-Schablone zur exakten Anpassung des autologen Knochentransplantats, das aus dem resezierten Humeruskopf entnommen wurde.
Die computergestützte 3D-Planung und die patientenspezifische Instrumentierung ermöglichen es der Chirurgin oder dem Chirurgen, die präoperative Planung während der Operation mit größerer Genauigkeit und Präzision umzusetzen und haben sich gegenüber der Standardinstrumentierung als überlegen erwiesen. Die klinischen Vorteile dieser Technologie, einschließlich einer verbesserten Langzeitüberlebensrate der Glenoidkomponente, einer geringeren Rate an Revisionsoperationen oder einer höheren Kosteneffektivität konnten wissenschaftlich noch nicht nachgewiesen werden [16].
Das Wichtigste in Kürze
Die Behandlung von Knorpelläsionen bleibt eine große Herausforderung. Die Mikrofrakturierung stößt bei größeren Läsionen an ihre Grenzen, daher hat sich die matrixassoziierte autologe Chondrozytenimplantation als Standardverfahren etabliert. Dieses zweizeitige Verfahren bringt allerdings einige entscheidende Nachteile mit sich, daher gewinnt die „Minced Cartilage“-Technik als einzeitiges Verfahren deutlich an Bedeutung. Sie ermöglicht es den Knorpeldefekt in nur einer Operation zu säubern, anzufrischen und mit autologem Knorpelzellmaterial aufzufüllen. Die Fixierung erfolgt mittels plättchenreichem Plasma (PRP) und autologem Fibrin. Daraus ergibt sich für den Patienten ein entscheidender Vorteil von einer kurzfristig möglichen, vollständig autologen Technik unter Verwendung moderner autologer biologischer Wirkstoffe.
Die robotische Assistenz im OP bietet eine Steigerung der Präzision und kann einen positiven Einfluss auf die Langlebigkeit von beispielhaft Teilendoprothesen nehmen.
Zusammenfassend bietet die 3D-Planung und PSI-Technologie einen erheblichen Mehrwert für die Patientensicherheit. Mithilfe der PSI-Technologie kann die Implantation von Glenoidkomponenten, sowohl bei anatomischen als auch inversen Prothesen, zuverlässig und korrekt durchgeführt werden. Vor allem bei deutlichen Deformitäten und ausgiebigen Knochensubstanzverlusten am Glenoid kann diese Technologie eine Hilfestellung bei der Planung sein und die optimale Ausrichtung der Glenoidkomponente präzise gewährleisten.
Die Autoren erklären, dass sie keine finanziellen oder persönlichen Beziehungen zu Dritten haben, deren Interessen vom Manuskript positiv oder negativ betroffen sein könnten.
Das Literaturverzeichnis kann im Internet unter www.bayerisches-aerzteblatt.de (Aktuelles Heft) abgerufen werden.
Autorin und Autoren

Professor Dr. Ralf Bieger
Franziska Warth
Professor Dr. Wolf C. Prall
Professor Dr. Florian Haasters
Artemed Klinikum München Süd, Zentrum für Knie-, Hüft-, Schulter und Ellenbogenchirurgie, Am Isarkanal 30, 81379 München


 Orthopädie und Unfallchirurgie
Orthopädie und Unfallchirurgie