Gefäßchirurgie heute
 Gefäßchirurgie heute
Gefäßchirurgie heute
Die moderne Gefäßchirurgie umfasst heutzutage die Diagnostik, die konservative, interventionelle und offen chirurgische Therapie sowie die Nachsorge vaskulärer Erkrankungen. Anhand von drei Kasuistiken sollen die Empfehlungen zur Diagnostik und Behandlung des infrarenalen Bauchaortenaneurysmas (European Society for Vascular Surgery – ESVS 2024, AWMF geplant 2026), akuter peripherer Gefäßverschlüsse (ESVS 2020, AWMF geplant 2026) und chronisch venöser Ulcerationen (ESVS 2022, AWMF 2024) vorgestellt werden.
Asymptomatisches infrarenales Bauchaortenaneurysma
Ein 67-jähriger Mann wird in der gefäßchirurgischen Sprechstunde mit dem Zufallsbefund eines asymptomatischen infrarenalen Aortenaneurysmas vorgestellt. In der Abdomensonografie im Rahmen des Aortenscreenings war eine fusiforme Aufweitung der infrarenalen Aorta auf 6 cm aufgefallen. An kardiovaskulären Risikofaktoren bestehen eine medikamentös behandelte arterielle Hypertonie sowie ein Nikotinabusus (ca. 30 pack years).
Ab einem Durchmesser von 30 mm, dies entspricht etwa dem 1,5-fachen des normalen Gefäßdurchmessers, wird von einem Bauchaortenaneurysma (AAA) gesprochen [1, 2]. Prävalenz und Inzidenz haben in den vergangenen 20 Jahren kontinuierlich abgenommen. Die schwedischen und britischen Screening-Programme zeigen aktuell Prävalenzen unter ein Prozent [3]. Ursächlich sind ein Rückgang des Nikotinkonsumes, die bessere Behandlung kardiovaskulärer Risikofaktoren und der Einsatz von Statinen und Thrombozytenaggregationshemmern [4, 5, 6]. Das jährliche Rupturrisiko liegt bei einem AAA < 5 cm bei ein Prozent oder weniger pro Jahr, bei einem AAA > 6 cm steigt das Risiko auf über 10 Prozent an [7]. Ein Screening wird in Deutschland seit 2017 einmalig als GKV-Leistung für alle Männer ab 65 Jahren angeboten. Für Frauen ab 65 Jahren empfiehlt die Deutsche Gesellschaft für Gefäßchirurgie (DGG) ein Screening bei aktueller oder früherer Raucheranamnese. Die ESVS hat aufgrund der Abnahme von Prävalenz und Inzidenz in den vergangenen Jahren die Empfehlung zum Screening in den aktuellen Leitlinien angepasst. Eine Ultraschalluntersuchung soll nun für Risikogruppen erfolgen. Als Risikofaktoren für das Vorhandensein eines AAA zählen männliches Geschlecht, Alter, Raucheranamnese, erstgradig Verwandte mit AAA, das Vorhandensein anderer peripherer Aneurysmen und Z. n. Organtransplantation [3].
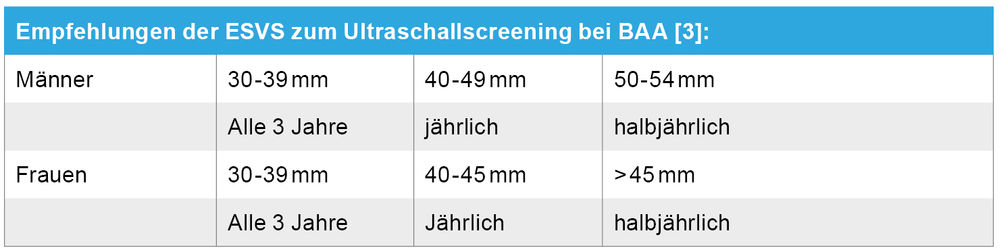
Die B-Bild-Sonografie ist die Methode der Wahl für das Screening und die Überwachung von AAA. Die Aorta wird im größten Durchmesser in a. p. – sowie transversaler Ebene orthogonal gemessen. In den deutschen Leitlinien wird die „leading edge-Methode“ empfohlen [8]. Für die Vergleichbarkeit von Messungen im Verlauf sollte die gleiche Messtechnik verwendet und dokumentiert werden. Die Überwachungsintervalle unterscheiden sich für Männer und Frauen [3], da die Wachstumsraten für beide Geschlechter zwar ähnlich sind und Frauen seltener erkranken, sie aber bei insgesamt kleineren Gefäßdurchmessern ein 4-fach höheres Rupturrisiko haben [3] (Tabelle 1).
Bei der Durchführung regelmäßiger Screenings sollten die Lebenserwartung, die anatomische Eignung zur Versorgung und die Patientenpräferenzen berücksichtigt werden. Falls es bei kleinen Aneurysmadurchmessern nicht zu erwarten ist, dass der Patient die Versorgungsgröße im Rahmen seiner Lebenserwartung erreicht oder er eine invasive Therapie ablehnt, sollte keine weitere Aneurysmaüberwachung erfolgen [3].
Eine CT-Angiografie (Abbildung 1) wird bei Erreichen des versorgungspflichtigen Durchmessers von 50 mm bei Frauen und 55 mm bei Männern empfohlen und nicht davor. Die Überversorgung kleiner Aneurysmen bei bekannt geringem Rupturrisiko soll so vermieden werden [3]. Mittels CT-Angiografie können die Anatomie und Morphologie der gesamten Aorta sowie der iliacalen und femoralen Zugangswege beurteilt werden und die Planung einer offenen Operation oder endovaskulären Stentversorgung (EVAR) erfolgen. Während in der älteren DGG-Leitlinie noch eine „kann“-Empfehlung für die Versorgung von AAA von 50 bis 54 mm besteht [8], rät die ESVS- Leitlinie aktuell klar davon ab [3]. Bei rascher Größenzunahme von > 10mm/Jahr wird von der ESVS eine erneute Kontrolle zur Überprüfung des Wachstums empfohlen, statt wie bisher in beiden Leitlinien unabhängig von der AAA-Größe die Therapie nahezulegen [9, 10, 11].
Unser Patient hat ein versorgungspflichtiges AAA mit 6 cm Durchmesser und ein klassisches Risikoprofil. Weitere kardiovaskuläre Risikofaktoren wie KHK, COPD oder Niereninsuffizienz werden mittels Anamnese, klinischer Untersuchung, EKG und Routinelabor ausgeschlossen. Es erfolgt eine CT-Angiografie der gesamten Aorta bis zu den Femoralgefäßen. Begleitende Popliteaaneurysmen werden sonografisch ausgeschlossen, ebenso Carotisstenosen. Die bestehende Medikation wird um ASS ergänzt. Offene Operation und endovaskuläre Versorgung werden mit dem Patienten ausführlich besprochen und bei anatomischer Eignung die Entscheidung zum endovaskulären Aortenrepair (EVAR) getroffen.
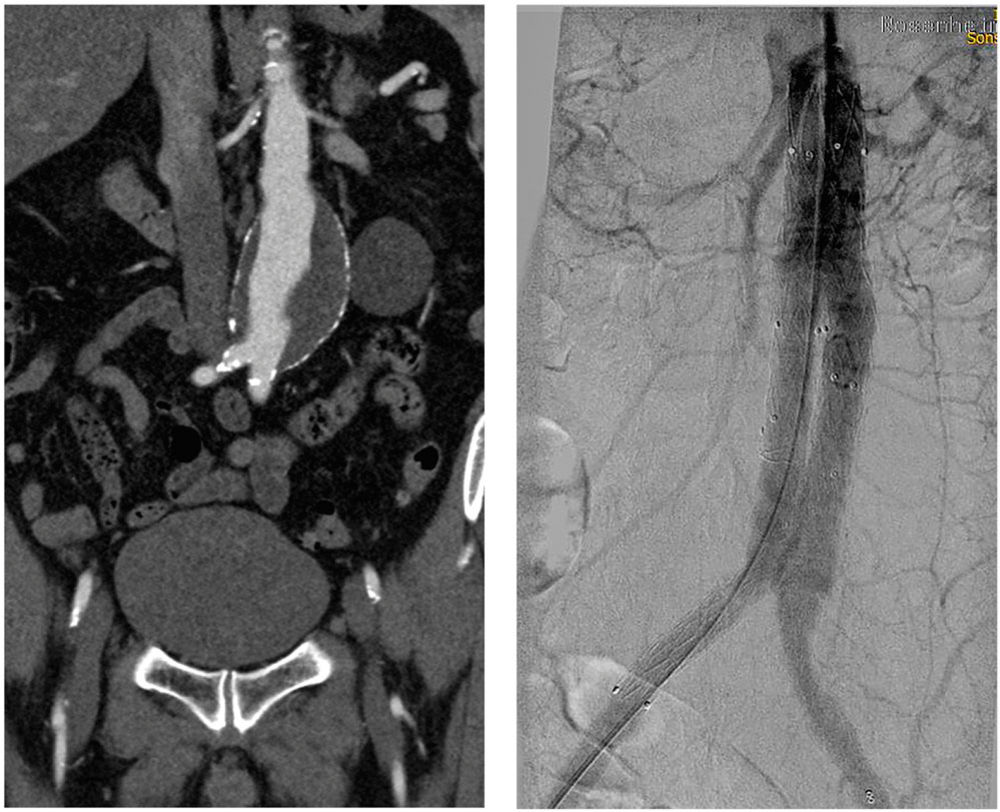 Abbildung 1 und 2: CT präoperativ und intraoperative Abschlussangiografie nach Implantation EVAR.
Abbildung 1 und 2: CT präoperativ und intraoperative Abschlussangiografie nach Implantation EVAR.
Die Versorgung des AAA erfolgt offen-chirurgisch (open repair – OR) oder mittels EVAR. Bei elektiver Behandlung intakter AAA wird individuell nach Alter, Lebenserwartung, Komorbiditäten, Aneurysma-Morphologie und Patientenwunsch entschieden. Vorteile von EVAR gegenüber OR sind die geringere Morbidität und Mortalität des Eingriffes, im Langzeitverlauf gleicht sich dies allerdings wieder an. Aktuell werden etwa 70 Prozent der intakten AAA mittels EVAR versorgt [57]. Die ESVS empfiehlt bei geeigneter Aneurysmamorphologie und akzeptabler Lebenserwartung primär EVAR, bei jungen Patienten mit langer Lebenserwartung sollte aber OR erwogen werden, da die Rate von Folgeeingriffen geringer und das „follow up“ weniger invasiv sind. Patienten mit einer Lebenserwartung unter zwei Jahren (terminale Tumorerkrankungen oder schwere Herzinsuffizienz) sollten nicht elektiv versorgt werden [3].
Nach entsprechender Vorbereitung und Planung nach CT-Angio wird bei geeigneter Anatomie eine komplikationslose perkutane EVAR-Versorgung mittels infrarenaler aortobiiliacaler Standardprothese durchgeführt. Intraoperativ zeigen sich keine „Endoleaks“ (undichte Stellen nach EVAR). Der Patient wird beschwerdefrei aus der stationären Behandlung in die strukturierte Nachsorge entlassen. Die Medikation besteht aus ASS, Statin und antihypertensiver Therapie, ein Nikotinverzicht wurde dringend empfohlen.
Nach EVAR ist in der Regel eine lebenslange Nachsorge notwendig, um krankheits- und implantatbedingte Komplikationen frühzeitig zu erkennen und zu behandeln. Die Intervalle unterscheiden sich je nach durchgeführter Versorgung (Standard-EVAR vs. komplexe, zum Beispiel fenestrierte Versorgung). Zur Verfügung stehen Duplexsonografie (DUS), kontrastmittelverstärkter Ultraschall (Contrast-Enhanced Ultrasound – CEUS), CT- und MR-Angio. Die ESVS empfiehlt primär die Durchführung einer CT-Angio innerhalb der ersten 30 Tage nach Implantation. Je nach Befund und Risikoprofil für Komplikationen kann dann über die weiteren Nachsorgeintervalle und -modalitäten entschieden werden. Die Nachsorge sollte durch das implantierende Zentrum erfolgen, bzw. festgelegt werden [3].
Nach OR dient die Nachsorge dem Ausschluss von Anastomosenaneurysmata und Stenosierungen sowie der Detektion einer weiteren Aneurysmaausdehnung nach proximal oder distal. Die Anastomosen können in der Regel gut mittels Ultraschall beurteilt werden. Eine CT- oder MR- Angio wird bei geringer Evidenz in Fünf-Jahres-Intervallen empfohlen.
Akute Extremitätenischämie (ALI)
Ein 75-jähriger Patient stellt sich mit einer seit zwei Tagen plötzlich bestehenden Claudicatio in der rechten Wade nach wenigen Metern Gehstrecke vor. An kardiovaskulären Risikofaktoren bestehen eine medikamentös behandelte arterielle Hypertonie, eine Hypercholesterinämie und ein Nikotinabusus. Klinisch ist der rechte Fuß im Seitenvergleich etwas kühler, die Rekapillarisationszeit ist verlängert, es besteht ein Kribbeln in den Zehen, die Motorik ist ungestört. Bei tastbaren Leistenpuls zeigt sich ein Pulsdefizit nach peripher bei unauffälligen Pulsstatus der Gegenseite. In der DUS zeigt sich in der distalen A. femoralis superficialis (AFS) ein thrombotischer Verschluss bei bereits arteriosklerotischen Veränderungen des Gefäßes. Mittels CT-Angiografie Aorta, Becken, Beine werden weitere Gefäßpathologien ausgeschlossen.
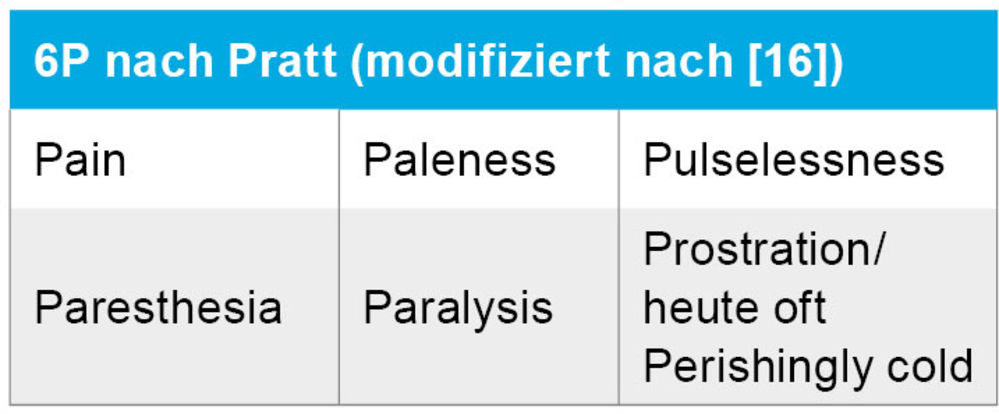
Von einer akuten Extremitätenischämie wird gesprochen, wenn die Symptomatik weniger als 14 Tage besteht. Die genaue Epidemiologie der ALI ist größtenteils aufgrund ihres heterogenen Erscheinungsbildes und der variablen Behandlungsarten unbekannt. Die meisten Studien und Daten liegen aus Westeuropa und Nordamerika vor [12]. Die Krankenhausinzidenz schwankt zwischen 5,1/100.000 Personen, bzw. 26,0/100.000 Personenjahre [12, 13, 14]. Etwa 50 Prozent werden offen chirurgisch versorgt und ca. 30 Prozent rein endovaskulär. Die Krankenhausmortalität liegt um neun Prozent, die Amputationsrate um sechs Prozent. Die Einjahres-Sterblichkeit liegt bei 40 Prozent und hat sich, im Gegensatz zu den vorgenannten Zahlen, über die Jahre nicht verbessert [12, 13, 14, 15]. Hauptursachen für ALI sind heutzutage Embolien aufgrund von kardialen Arrhythmien, Thrombosierungen in vorbestehenden arteriosklerotischen Veränderungen und iatrogen verursachte Gefäßverschlüsse [12]. Die „6P“ nach Pratt (Tabelle 2) beschreiben die klinische Präsentation. Im Vollbild sind sie in der Regel bei einem akut embolischen, iatrogenen oder traumatischen Verschluss ohne vorbestehende arteriosklerotische Veränderung und damit fehlender Kollateralenbildung zu sehen (Tabelle 2).
Patienten mit einer akuten Extremitätenischämie sollten einem Gefäßspezialisten vorgestellt werden und die bildgebende Diagnostik sollte die notwendige Behandlung nicht verzögern [12]. Geeignet sind DUS und die CT-Angiografie (CT-A) als Goldstandard bei breiter Verfügbarkeit und schneller Evaluation des gesamten Gefäßstatus. Die MR-Angiografie ist möglich, aber in der Regel nicht flächendeckend schnell verfügbar. Die digitale Subtraktionsangiografie (DSA) zur alleinigen Diagnostik ist heutzutage obsolet. Laborwerte wie Kreatinkinase (CK), Myoglobin und Laktat dienen als Marker eines Gewebeschadens, bzw. einer Rhabdomyolyse. Sie werden im perioperativen Management zur Abschätzung eines Reperfusionsödemes oder Notwendigkeit einer frühen Fasziotomie herangezogen. Eine Entscheidung über Therapie oder Amputationsrisiko anhand von Laborwerten wird aber nicht empfohlen [12, 17, 18].
Die initiale Therapie umfasst eine adäquate Analgesie sowie die Gabe von unfraktioniertem Heparin (UFH), initial als Bolus von 5.000 IE oder als kontinuierliche Infusion von 70 bis 100 IE/kg KG [12].
Bei Rutherford-Stadium IIa mit moderater Symptomatik und Nachweis eines thrombotischen Verschlusses der rechten AFS in DUS und CT-A wird bei unserem Patienten nach sonogesteuerter antegrader Punktion der A. femoralis communis rechts und Angiografie eine interventionelle Therapie mittels kathetergestützter lokaler Lysetherapie mit Alteplase/rt-PA eingeleitet. Nach 24 Stunden Lysetherapie unter intensivmedizinischer Überwachung zeigt sich in der Angiokontrolle eine vollständige Auflösung des Thrombus mit Demaskierung einer hochgradigen Stenose der distalen AFS im Adduktorenkanal bei Dreigefäßabstrom nach peripher. Der Befund kann komplikationslos mittels drug eluting-PTA (DEB) nach Vordilatation behandelt werden. Eine duale Thrombozytenaggregationshemmung (TAH) mit ASS und Clopidogrel wird eingeleitet und vor Entlassung sonografisch ein Aneurysma spurium der Punktionsstelle ausgeschlossen.
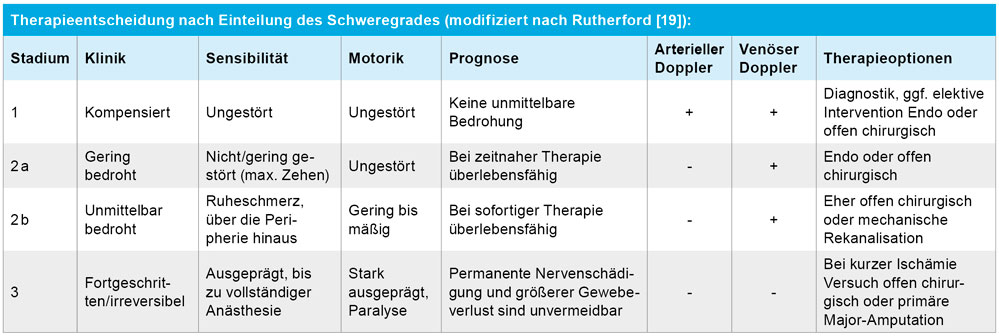
Die Wahl des Therapieverfahrens richtet sich individuell nach dem Schweregrad der Ischämie anhand der Rutherford-Klassifikation, der Genese des Verschlusses, Kontraindikationen sowie dem Allgemeinzustand und der Präferenz des Patienten. Idealerweise erfolgt die Behandlung in einem vaskulären Zentrum, in dem operative und endovaskuläre Therapie 24/7 angeboten werden können [12] (Tabelle 3). Bei embolischen Verschlüssen mit ausgeprägter Ischämie ist die operative Therapie mit Katheterembolektomie nach Fogarty zur schnellen Revaskularisation das Mittel der Wahl [20]. Unter Röntgenkontrolle kann die Sondierung cruraler Gefäße mittels Drahtes als „over-the-wire-Embolektomie“ erfolgen. Die intraoperative angiografische Kontrolle ist obligat [12]. Eine Kombination chirurgischer und interventioneller Techniken kann als Hybrid-Chirurgie erfolgen. Bei milder Klinik kann wie in unserem Fallbeispiel – nach Ausschluss von Kontraindikationen – die perkutane intraarterielle Lysetherapie mit anschließender Intervention durchgeführt werden. In den vergangenen Jahren haben sich verschiedene endovaskuläre Techniken zur mechanischen Rekanalisation etabliert, um mittels Thrombusaspiration und/oder -fragmentation die Thrombuslast im Rahmen eines weniger invasiven perkutanen Eingriffes zügiger zu reduzieren und die Perfusion wieder herzustellen. So können auch Rutherford-Stadien IIb alternativ zum chirurgischen Vorgehen schnell minimalinvasiv behandelt werden. Vorteile sind eine geringere Invasivität und Belastung für den Patienten. Nachteile können nicht ausreichende Thrombusentfernung, lokale Gefäßverletzung und periphere Embolisation sein. Nachdem sich in älteren Auswertungen keine signifikanten Vorteile für OP oder endovaskuläre Techniken bezüglich Mortalität und Beinerhalt gezeigt haben [21 bis 25], lassen sich in neueren schwedischen und französischen Arbeiten Vorteile hinsichtlich der modernen endovaskulären Verfahren nachweisen [26, 27].
Die Nachsorge beinhaltet bei embolischem Verschluss die Emboliequellensuche und Antikoagulation. Bei thrombotischem Verschluss in arteriosklerotisch veränderten Gefäßen erfolgt die optimale Einstellung der kardiovaskulären Risikofaktoren mittels best medical treatment mit TAH und Statin sowie die Empfehlung zum Nikotinverzicht.
Ulcus cruris venosum
Eine 70-jährige Patientin stellt sich in der gefäßchirurgischen Sprechstunde mit einem seit vier Wochen erstmalig bestehenden Ulcus am distalen medialen Unterschenkel rechts vor. Anamnestisch lassen sich weder Thrombose noch Venenoperationen in der Vorgeschichte erfragen. In der klinischen Untersuchung zeigen sich ein regelrechter Pulsstatus, eine sichtbare Varikose am medialen Unterschenkel, ein geringes Ödem des Unterschenkels mit Hyperpigmentierung und ein ca. 3x4 cm großes, kaum belegtes Ulcus mit schuppiger Wundumgebung kranial des Malleolus medialis.
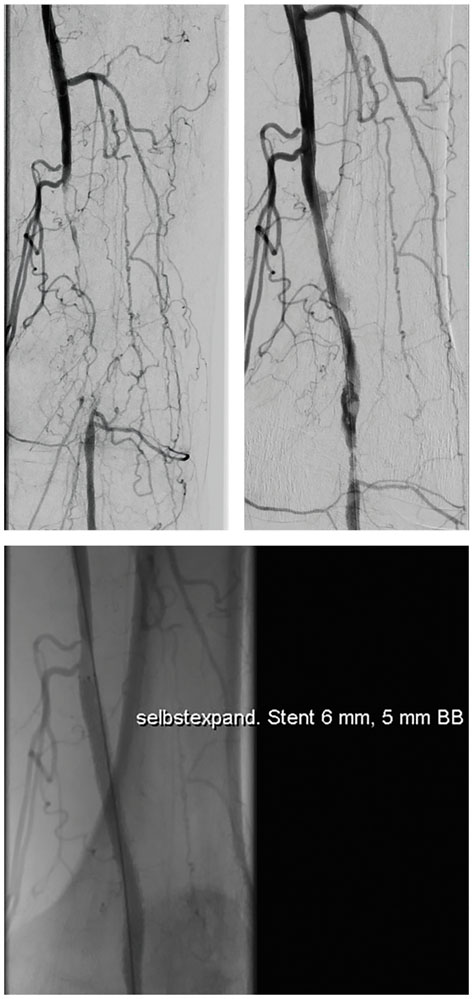
Abbildung 3 bis 5: Bilder zu einem akuten Gefäßverschluss A. femoralis superficialis/A. poplitea. Angio mit Verschluss, Angio nach Lyse mit Stenose, Angio nach Stentimplantation.
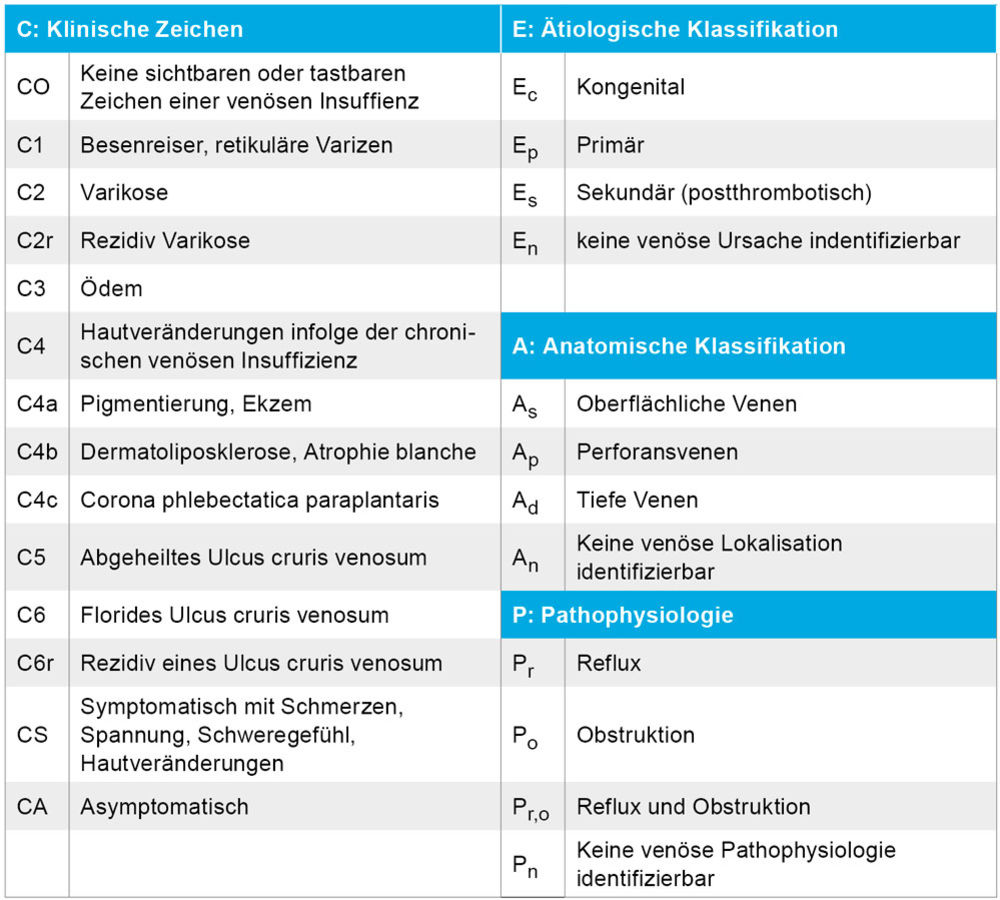
Das Ulcus cruris venosum (UCV) ist die schwerste Verlaufsform einer chronisch venösen Insuffizienz (CVI) und wird nach der CEAP-Klassifikation als C5 (abgeheilt) oder C6 (floride) eingeteilt (Tabelle 4) [28]. Eine CVI entsteht durch Hochdruck im venösen System, der entweder durch Reflux oder Obstruktion oder eine Kombination beider verursacht wird. Das UCV ist für 50 bis 80 Prozent der vaskulären Ulcera verantwortlich, in 10 bis 15 Prozent liegt ein arterielles Ulcus (UCA), in 10 bis 13 Prozent ein Ulcus gemischt arterieller und venöser Genese, vormals Ulcus cruris mixtum (UCM) und in 20 Prozent ein Ulcus anderer Ursache vor [29]. Die Prävalenz des floriden UCV wird mit 0,1 bis 0,3 Prozent angegeben und beträgt bei über 80-jährigen etwa zwei Prozent [30, 31]. Die Rezidivrate ist hoch. Risikofaktoren für die Entstehung eines UCV sind familiäre Disposition, hohes Lebensalter, Adipositas, Varikosis und das postthrombotische Syndrom (PTS).
Detaillierte Anamneseerhebung und klinische Untersuchung mit Inspektion und Palpation bilden die Basis der Diagnostik [32]. Bei Hinweisen auf eine nicht rein venöse Genese des Ulcus soll diese weiter abgeklärt werden. Der arterielle Status sollte mittels Erfassung der Pulse und ABI-Messung erfolgen. Bereits in der Ersterfassung sollte eine farbkodierte Duplexsonografie (DUS) der Beinvenen erfolgen. Adäquate Wund- und Kompressionstherapie sollen ohne Zeitverzögerung eingeleitet werden, auch schon vor erfolgter DUS [29]. Bei ausbleibender Heilungstendenz trotz adäquater sechswöchiger Therapie wird eine Reevaluation mit ggf. Entnahme von Gewebebiopsien zur histologischen Untersuchung empfohlen [33]. Die Prävalenz von Neoplasien beträgt im Ulcus cruris zwei bis 10 Prozent [34].
In der DUS zeigt sich eine Insuffizienz der V. saphena magna bei suffizientem und freiem tiefen Venensystem. Nach initialer Entstauung mittels phlebologischen Kompressionsverbands (PKU) Wechsel auf ein Oberschenkel-Ulcusstrumpfsystem Kompressionsklasse (CCL) 2 (Abbildung 6). Zur kausalen Therapie der oberflächlichen Veneninsuffizienz erfolgen ambulant eine Crossektomie mit Stripping der V. saphena magna bis Hach III sowie eine Miniphlebektomie der Seitastvarikose. Unter Fortführung der Kompressionstherapie heilt das Ulcus unter stadiengerechter Wundtherapie innerhalb von drei Wochen ab.
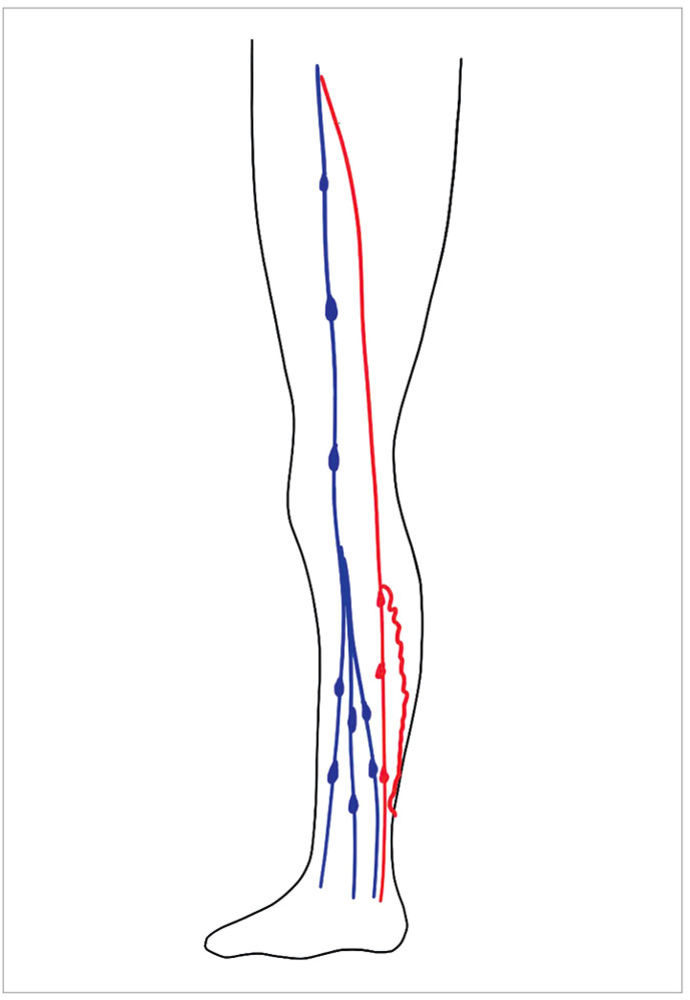
Abbildung 6: Insuffizienz V. saphena magna Hach III mit Seitastvarikose Unterschenkel medial
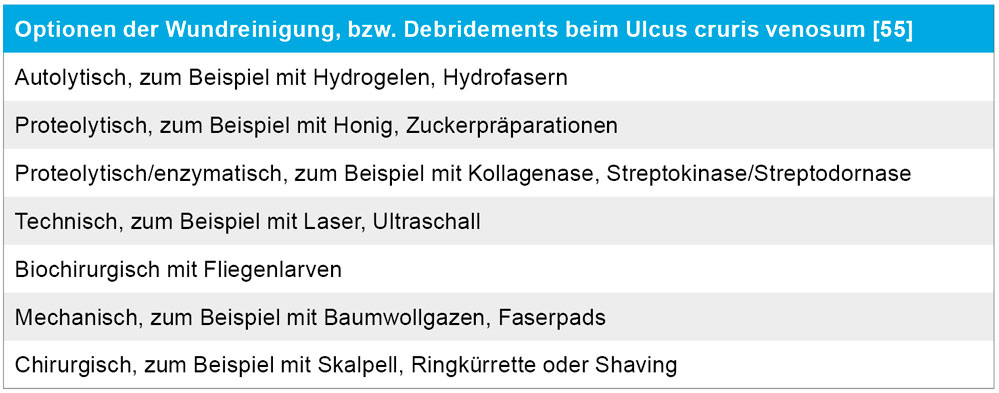
Die Therapie des UCV beinhaltet als Basismaßnahmen immer die stadiengerechte Wundtherapie und Kompression. Ziel ist eine schmerzarme Wundversorgung mit Debridement, Exsudatmanagement sowie Abdeckung der Wunde. Bei lokaler Infektion können Antiseptika eingesetzt werden und es sollen Wundabstriche zur Erregerdiagnostik und Resistenzbestimmung vor systemischer Antibiose erfolgen. Lokale antibiotische Behandlungen werden nicht empfohlen. Bei reizlosem Ulcus ist ein Wundabstrich nicht erforderlich. Eine reine Kolonisierung wird nicht behandelt.
Die Kompressionstherapie wird in der S2k-Leitlinie der AWMF „Medizinische Kompressionstherapie der Extremitäten mit Medizinischem Kompressionsstrumpf (MKS), Phlebologischem Kompressionsverband (PKV) und Medizinischen adaptiven Kompressionssystemen (MAK)“ ausführlich erläutert und soll nach Prüfung von Kontraindikationen immer eingesetzt werden [35]. Die Abheilung wird damit klar beschleunigt.
Kontraindikationen für die medizinische Kompressionstherapie:
- Fortgeschrittene arterielle Durchblutungsstörung (pAVK) (ABI < 0,5, Knöchelarteriendruck < 60mmHg, Zehendruck < 30mmHg oder TcPO2 < 30 mmHg am Fußrücken)
- Dekompensierte Herzinsuffizienz (NYHA 3 und 4)
- Phlegmasia coerulea dolens
Eine Kompressionstherapie sollte auch bei begleitender pAVK eingesetzt werden [36, 37, 38]. Durch die Kompression, ggf. mit verringertem Anpressdruck auf 20 mmHg (CCL1), kommt es zu einer Verbesserung der transkutanen Sauerstoffpartialdruckmessung (TcPO2) in der Wundumgebung und des arteriellen Blutflusses. PKV werden initial in der Entstauungsphase verwendet und sollten 24 Stunden getragen werden. In der Erhaltungstherapie bieten sich zweiteilige Ulkus-Kompressionsstrumpfsysteme an. Der Tragekomfort ist hoch und der Anpressdruck stabil im Vergleich zu PKV [39, 40]. Anziehhilfen können und sollten bei Bedarf verordnet werden. Als Alternativen für die Entstauungs- wie auch Erhaltungsphase bieten sich MAK an. Dies sind modulare Kompressionssysteme, die den Patienten ein leichtes Anlegen mit korrektem Anpressdruck ermöglichen [41, 42]. Patienten sollen zu regelmäßiger körperlicher Aktivität angehalten werden, um die Muskel- und Gelenkpumpe zu aktivieren. Bei begleitendem Lymphödem soll eine komplexe Entstauungstherapie erfolgen. Bei Adipositas ist eine Gewichtsreduktion anzustreben.
Die invasive Therapie dient der kausalen Behandlung der venösen Hypertonie. Bei venöser Insuffizienz im oberflächlichen Venensystem soll dies frühzeitig erfolgen, um eine schnelle Abheilung und eine Senkung des Rezidivrisikos zu erreichen [43, 44]. In der EVRA-Studie konnte gezeigt werden, dass eine frühere Intervention bei noch bestehendem Ulcus zu einer schnelleren Ulcusabheilung führte [45]. In der ESCHAR-Studie zeigte sich ein geringeres Rezidivrisiko nach Operation plus Kompression im Vergleich zu alleiniger Kompression (31 Prozent vs. 56 Prozent) [46]. Ob ein klassisches chirurgisches Verfahren oder eine endovenöse Therapie erfolgen, soll abhängig vom konkreten Befund und nach Nutzen-Risiko-Abwägung mit dem Patienten abgestimmt werden. Auch bei begleitender Leitveneninsuffizienz mit Reflux im tiefen Venensystem soll nach Ausschluss einer Obstruktion eine invasive Behandlung der oberflächlichen Veneninsuffizienz erfolgen, da sich darunter die klinische Symptomatik bessert und eine Ulcusabheilung erreicht werden kann. Bei Patienten mit UCV und relevanter pAVK sollen beide Erkrankungen leitliniengerecht behandelt werden. Es muss individuell entschieden werden, welche Erkrankung im Vordergrund steht und primär behandelt wird [38, 47, 48, 49, 50].
Bei Obstruktionen der Beckenvenen kann eine invasive Therapie mittels Angioplastie oder Stentimplantation in Betracht gezogen werden, wenn es einen ursächlichen Zusammenhang gibt. Die Behandlung soll in einem dafür spezialisierten Zentrum immer in Kombination mit einer Kompressionstherapie und nach Ausschöpfung sämtlicher ulcusrelevanter Therapieoptionen im oberflächlichen Venensystem erfolgen [51 bis 54].
Die lokale Wundtherapie beinhaltet schmerzarme Verbandwechsel mit lokalen Debridements. Hierfür stehen verschieden invasive Techniken wie zum Beispiel die Shave-Therapie mit zeitgleicher Defektdeckung mittels Spalthaut zur Verfügung [29] (Tabelle 5).
Die Nachsorge und Rezidivprophylaxe beinhalten die Patientenedukation mit Bewegungstraining, Gewichtsnormalisierung und Fortführung der Kompressionstherapie. Um die Therapieadhärenz zu erhöhen, kann langfristig ggf. auf einen Wadenstrumpf CCL 1 gewechselt werden [29, 56].
Die Autoren erklären, dass sie keine finanziellen oder persönlichen Beziehungen zu Dritten haben, deren Interessen vom Manuskript positiv oder negativ betroffen sein könnten.
Das Literaturverzeichnis kann im Internet unter www.bayerisches-aerzteblatt.de (Aktuelles Heft) abgerufen werden.
Autorin und Autoren

Dr. Andrea van Dyck, Oberärztin Gefäßchirurgie
Petar Viktorov, Oberarzt Gefäßchirurgie

Professor Dr. Kai Nowak, Chefarzt Allgemein-, Gefäß- und Thoraxchirurgie
RoMed Klinikum Rosenheim, Ellmaierstraße 23, 83022 Rosenheim, Internet: www.romed-kliniken.de
Teilen:
Das könnte Sie auch interessieren: