Anstrengungen der Tiermedizin zur Reduktion von Antibiotikaresistenzen
 Künftige Kategorisierung von Antibiotika in der Tiermedizin.
Künftige Kategorisierung von Antibiotika in der Tiermedizin.
Der Erhalt der Wirksamkeit antimikrobieller Wirkstoffe wurde von der WHO zur größten Herausforderung der Medizin im 21. Jahrhundert ausgerufen. Als Ursache für die zunehmende Resistenzproblematik in der Humanmedizin wird in der öffentlichen Diskussion häufig der leichtfertige und übermäßige Einsatz von Antibiotika in der Tiermast genannt. Doch stimmt das wirklich? Werden landwirtschaftliche Nutztiere immer noch mit Antibiotika gemästet? In der Tat gehören derlei Vorstellungen der Vergangenheit an. Denn der Gesetzgeber hat das Problem früh erkannt und die Antibiotikaanwendung in der Tiermedizin durch strikte arzneimittelrechtliche Vorgaben auf ein heute medizinisch notwendiges Mindestmaß reduziert. Der folgende Artikel gibt einen Überblick über die Entwicklung des derzeitigen Rechtsrahmens und zeigt die Erfolge aber auch Grenzen der Reduktion von Antibiotika in der Tiermedizin auf.
In ihrem „Review on Antimicrobial Resistance“ beziffert der Wellcome Trust die weltweite Sterblichkeit aufgrund von Infektionen mit resistenten Keimen im Jahr 2014 auf ca. 700.000 Todesfälle. Ohne ein radikales Umdenken in der Verordnungspraxis von Antibiotika würde die Sterblichkeit im Jahr 2050 auf ca. 10 Millionen Todesfälle weltweit ansteigen [1]. Für die Bundesrepublik Deutschland veröffentlichte das European Antimicrobial Resistance Surveillance Network (ERAS-Net) [2] kürzlich aktuelle Zahlen für das Jahr 2017. Demnach wurden in Krankenhäusern ca. 54.500 Patienten mit resistenten Infektionserregern behandelt, wovon ca. 2.400 Menschen starben. In den öffentlichen Medien wie der zuletzt am 12. März 2019 in ARTE ausgestrahlten TV-Reportage „Resistance Fighters – die globale Antibiotika Krise“ werden die Schuldigen hierfür schnell gefunden. Es sind die Tierärzte, die „insbesondere durch den Einsatz selbst kostbarer Reserve-Antibiotika als Wachstumsbeschleuniger in der Tiermast“ die Entwicklung von Multiresistenzen fördern [3]. Derart pauschale Schuldzuweisungen sind so falsch wie gefährlich, denn sie lenken vom eigentlichen Problem ab. Die Resistenzproblematik ist ein globales, multifaktorielles Problem, das nur im Sinne des „One-Health-Ansatzes“ durch gemeinsame Aktionen aller beteiligten Personenkreise aus Landwirtschaft, Lebensmittelindustrie, Tiermedizin, Humanmedizin und öffentlichen Gesundheitswesen gelöst werden kann [4]. Die Politik hat dabei schon früh die besondere Verantwortung der Tierärzte bei der Anwendung von Antibiotika erkannt. Bereits lange bevor das Thema durch die Veröffentlichung der ersten Globalen Strategie zur Eindämmung von Antibiotikaresistenzen durch die WHO [5] im Jahr 2001 in das öffentliche Bewusstsein gelangte, hat der Gesetzgeber auf nationaler Ebene begonnen, die Mindestanforderungen an die Arzneimittelverordnung über arzneimittelrechtliche Vorschriften zu regulieren.
Mit der Einführung detaillierter Regelungen zur Diagnostik, Arzneimittelauswahl, Anwendung und Dokumentation sowohl beim Kleintier als auch bei Lebensmittel liefernden Tieren hat die Entwicklung des nationalen Arzneimittelrechts im Jahr 2018 ihren Abschluss erreicht. Im Folgenden werden die wichtigsten Meilensteine bis zum heutigen Rechtsrahmen dargestellt (Abbildung 1):
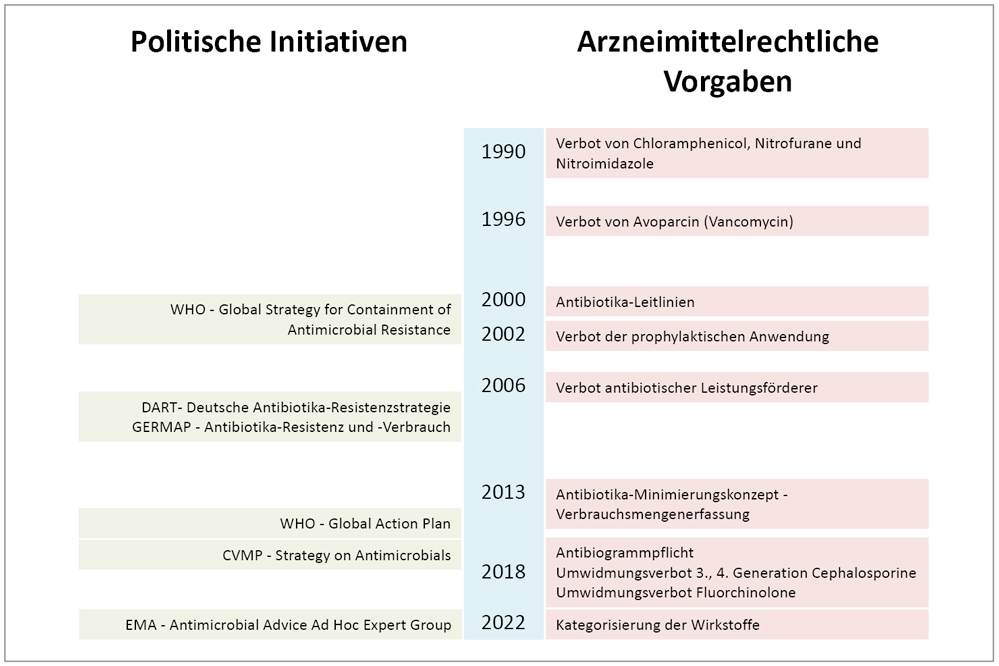
Abbildung 1: Entwicklung arzneimittelrechtlicher Bestimmungen für die Tiermedizin.
Der Humanmedizinische Vorbehalt
Im Jahr 1990 wurden mit der VO (EG) 2377/90 erstmals in der Europäischen Gemeinschaft für alle Mitgliedsstaaten bindende Regelungen für die Anforderungen an Arzneimittel eingeführt, die bei Lebensmittel liefernden Tieren eingesetzt werden [6]. Der zugrundeliegende Gedanke war, die Bevölkerung im Sinne des vorbeugenden Verbraucherschutzes vor einer gesundheitlichen Gefährdung durch Tierarzneimittelrückstände zu schützen. Auf Antibiotika bezogen wurden zunächst diejenigen Wirkstoffe verboten, deren Rückstände beim Verbraucher toxische Wirkungen auslösen können. Darunter fielen potenziell kanzerogene Stoffe wie Chloramphenicol, Nitrofurane und Nitroimidazole. Darüber hinaus wurden sogenannte mikrobiologische Rückstandshöchstmengen für Lebensmittel tierischen Ursprungs eingeführt, die beim Verbraucher die Selektion resistenter Keime durch Antibiotikarückstände verhindern sollen. Schließlich wurde als dritte Maßnahme ein Zulassungsverbot für neue Wirkstoffgruppen in der Tiermedizin eingeführt. Seither bleiben neue Antibiotika ausschließlich der Humanmedizin vorbehalten.
Verbot antibiotischer Leistungsförderer
Antibiotische Leistungsförderer waren Futtermittelzusatzstoffe, die in subtherapeutischen Dosierungen zur Verbesserung der Futterverwertung verabreicht wurden. Um die Gefahr der Bildung Vancomycin-resistenter Enterokokken vorzubeugen, wurde zum 21. Januar 1996 auf nationaler Ebene die Anwendung von Avoparcin, einem strukturverwandten Glykopeptid verboten [7]. Ziel der Maßnahme war es, die Wirksamkeit von Vancomycin und Teicoplanin bei Darminfektionen in der Humanmedizin zu bewahren. Auf europäischer Ebene lief zum 1. Januar 2006 die Verschreibungsfähigkeit der letzten vier antibiotischen Leistungsförderer (Monensin, Salinomycin, Avilamycin, Falvophospholipol) aus [8]. Seither werden per definitionem keine Antibiotika zur Steigerung der Mastleistung eingesetzt.
Stärkung der tierärztlichen Verordnungspraxis
Die besondere Verantwortung der Tierärzte bei der Verordnung von Antibiotika wurde im Jahr 2000 mit der Veröffentlichung der Leitlinien für den sorgfältigen Umgang mit antibakteriell wirksamen Tierarzneimitteln [9] umgesetzt. Diese wurden von der Bundestierärztekammer und der Arbeitsgemeinschaft der Leitenden Veterinärbeamten der Länder (ArgeVet) herausgegeben und legen die Mindestanforderungen an Diagnostik, Auswahl und Anwendung von Antibiotika bei allen Tierarten fest. Obwohl sie keinen Gesetzescharakter besitzen, definieren sie den derzeitigen Stand der veterinärmedizinischen Wissenschaften.
Mit dem 11. Gesetz zur Änderung arzneimittelrechtlicher und anderer Vorschriften (AMG-Novelle) [10] wurde zum 1. September 2002 als Reaktion auf den letzten großen Schweinemastskandal ein umfangreiches Maßnahmenpaket zur Gewährleistung des sachgemäßen Umganges mit Antibiotika erlassen. Die einzelnen Regelungen umfassten die Beschränkung der Verordnungspraxis auf ausschließlich medizinisch begründbare Indikationen, ein Herstellungsverbot für Fütterungsarzneimittel, ein Abgabeverbot für Arzneimittelvormischungen, die Einführung des Zulassungsprimates und die Beschränkung der Abgabemenge systemisch wirksamer Antibiotika für einen Zeitraum von maximal sieben Tagen. Mit diesen Regelungen wurde erstmals die Forderung nach einer Reduktion der verordneten Arzneimittelmengen umgesetzt und der prophylaktische Einsatz von Antibiotika abgeschafft. Durch das Zulassungsprimat dürfen Arzneimittel nur noch bei den in den Zulassungsbedingungen genannten Tierarten und Indikationen eingesetzt werden. Jede Abweichung hiervor erfordert einen medizinisch begründeten Therapienotstand.
Antibiotikum-Minimierungskonzept
Mit der zum 5. Juli 2013 in Kraft getretenen 16. AMG-Novelle [11] wurden schließlich die Vorgaben der Deutschen Antibiotika-Resistenzstrategie (DART) zur Reduktion des Antibiotikaverbrauchs durch Verbesserung der Haltungsbedingungen und Tierhygiene umgesetzt. Im Zentrum steht die kontinuierliche Erfassung der verordneten Antibiotikamengen durch Landwirte, die Rinder, Schweine, Hühner und Puten zur Mast halten. Durch den bundesweiten Vergleich des Antibiotikaverbrauchs können Tierhalter identifiziert werden, die überdurchschnittlich häufig Antibiotika einsetzen. Diese müssen gegebenenfalls unter Mitwirkung eines Tierarztes sogenannte Maßnahmenpläne erarbeiten, in denen sie die Gründe für die erhöhte Anfälligkeit für Infektionskrankheiten identifizieren und geeignete Verbesserungsmaßnahmen vorschlagen. Damit soll die Behandlungshäufigkeit nachhaltig verringert werden.
Kontrollierter Einsatz von Reserveantibiotika
Als letzte Anpassungen im nationalen Arzneimittelrecht traten zum 1. März 2018 mit dem 2. Gesetz zur Neufassung der tierärztlichen Hausapothekenverordnung (TÄHAV) [12] detaillierte Anforderungen an die Anfertigung und Durchführung von Antibiogrammen, ein Umwidmungsverbot für Cephalosporine der 3. und 4. Generation und für Fluorchinolone sowie weiterführende Aufzeichnungspflichten bei der Verordnung von Antibiotika in Kraft. Die Vorgaben verfolgen das Ziel, die Anwendung von antibiotischen Reservemittel in Tierbeständen zu reduzieren und ihre Wirksamkeit zu garantieren.
Die umfangreichen arzneimittelrechtlichen Vorgaben an die Arzneimittelverordnung schränken einerseits die individuelle Therapiefreiheit weitgehend ein, sie bieten den Tierärzten bei der Umsetzung der Anforderungen an eine rationale Antibiose aber auch die nötige Rechtssicherheit. Tierärzte sind Kraft ihrer Approbation dazu verpflichtet, Infektionskrankheiten bei Tieren zu verhindern oder zu heilen [13]. Hierfür stehen ihnen jedoch aus pharmakologischer Sicht keine eigenen Stoffgruppen zur Verfügung. Sie müssen vielmehr auf dieselben antimikrobiellen Wirkstoffe zurückgreifen, die auch in der Humanmedizin eingesetzt werden. Es ist daher unvermeidlich, dass durch die Antibiotikaanwendung beim Tier resistente Krankheitserreger entstehen, die entweder direkt oder indirekt auf den Menschen übertragen werden können. Das mit der 16. AMG-Novelle implementierte Antibiotikum-Minimierungskonzept hat zweifelsohne zu einer starken Reduktion der Verordnungsmengen geführt [14]. Aktuelle Daten des Bundeslandwirtschaftsministeriums zur Evaluation des Antibiotikum-Minimierungskonzeptes legen jedoch eine Erschöpfung des Einsparpotenzials vor allem in der Hühner-, Puten- und Kälbermast nahe. Gleichzeitig scheinen die Vorgaben zur Antibiotikaeinsparung aber auch mit Veränderungen in der Verordnungspraxis einherzugehen. Mengenmäßig häufig eingesetzte einfache Wirkstoffe werden offenbar durch besser wirksame Fluorchinolone ersetzt oder wie bei Colistin in höheren Dosierungen verordnet [15].
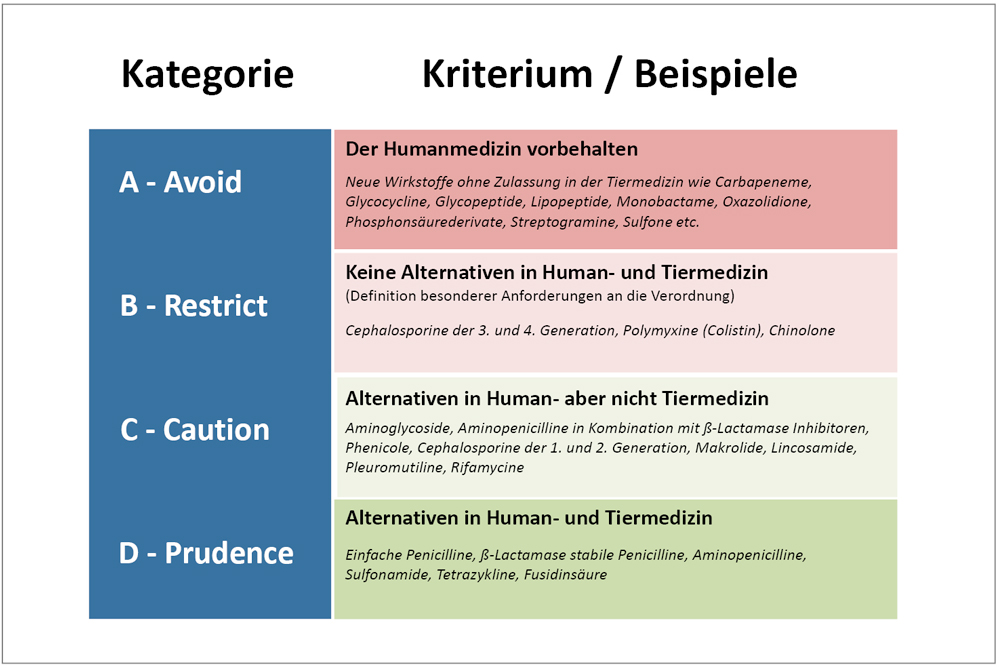
Welche weiteren Strategien zum Erhalt der Wirksamkeit von Antibiotika in der Humanmedizin sind geplant? Mit Inkrafttreten der Europäischen Tierarzneimittelverordnung VO (EU) 2019/6 zum 28. Januar 2022 wird als vorläufig letzte Änderung eine Priorisierung der Wirkstoffe hinsichtlich ihrer Bedeutung für die Humanmedizin umgesetzt [16]. Die Kategorisierung orientiert sich an der WHO-Liste von „Critically Important Antibiotics for Human Medicine“ [17], berücksichtigt aber auch die von der World Organization of Animal Health (OIE) definierten Anforderungen an den Antibiotikaeinsatz in der Tiermedizin [18]. Ziel ist es, nur noch solche antimikrobiellen Wirkstoffe einzusetzen, von denen nur eine geringe Gefahr für Antibiotikaresistenzen ausgeht und für die in der Humanmedizin ausreichend Alternativen vorliegen (Abbildung 2).

Abbildung 2: Künftige Kategorisierung von Antibiotika in der Tiermedizin.
Fazit
Der vorliegende Artikel zeigt, dass die Antibiotikaanwendung in der Tiermedizin unter der Maßgabe des Schutzes der Bevölkerung vor Antibiotikaresistenzen erfolgt. Der derzeitige Rechtsrahmen gewährleistet den sorgsamen Umgang mit Antibiotika durch Tierärzte und reduziert ihn auf ein medizinisch gerechtfertigtes Mindestmaß. Heute immer noch häufig vorgebrachte Argumente die Tierärzte würden als Erfüllungsgehilfen der Landwirte große Mengen an Antibiotika verordnen, sind nicht mehr zeitgemäß und gehören der Vergangenheit an. Unter dem Dach des Bayerischen Aktionsbündnis gegen Antibiotikaresistenz (BAKT) unternehmen in Bayern die Landesarbeitsgemeinschaft Multiresistente Erreger (LARE) und die Arbeitsgemeinschaft Resistente Erreger in der Veterinärmedizin (ARE-Vet) große Anstrengungen, im Sinne des One-Health-Ansatzes die fachspezifischen Besonderheiten im Umgang mit Antibiotika zwischen Human- und Tiermedizin zu kommunizieren. Nur durch Kenntnis der Möglichkeiten und Grenzen der Antibiotikaeinsparung im jeweiligen Fachgebiet können künftige Strategien zur Resistenzminimierung erfolgreich umgesetzt werden.
Autoren
Dr. med. vet. Maximilan Muehlhaupt
Professor Dr. med. vet. Hermann Ammer 1
Korrespondenadresse:
1 Institut für Pharmakologie, Toxikologie und Pharmazie, Veterinärwissenschaftliches Department, Tierärztliche Fakultät, Ludwig-Maximilians-Universität München, Königinstraße 16, 80539 München, E-Mail: h.ammer(at)lmu.de
Teilen:
Das könnte Sie auch interessieren: