Entzündlich rheumatische Erkrankungen heute
 Rheumatologie
Rheumatologie
Drei häufige Kasuistiken aus der rheumatologischen Praxis und was sich in den vergangenen Jahren geändert hat
In Deutschland leben etwa zwei Millionen Menschen mit entzündlich-rheumatischen Erkrankungen [1]. Während bei diesen Diagnosen früher langfristige Beeinträchtigungen drohten, haben Fortschritte in Diagnostik und Therapie den Krankheitsverlauf in den vergangenen Jahrzehnten grundlegend verändert. Seit der Einführung krankheitsmodifizierender Therapien DMARDs (Disease-Modifying Antirheumatic Drugs) in den späten 1980er- und 1990er-Jahren lassen sich entzündlich-rheumatische Erkrankungen heute gezielt behandeln und bei vielen Patientinnen und Patienten in Remission bringen [2]. Seit Ende der 1990er-Jahre haben Biologika die therapeutischen Möglichkeiten erweitert, während sich der Ultraschall als zentrales Instrument der rheumatologischen Diagnostik etabliert hat [3].
Eine spannende neue Perspektive stellen zellbasierte Therapiekonzepte wie Chimäre Antigen-Rezeptor-T-Zellen (CAR-T-Zellen) dar, die 2022 erstmalig am Universitätsklinikum Erlangen für rheumatische Erkrankungen eingesetzt wurden. Erste Daten aus frühen Studienphasen deuten darauf hin, dass bei ausgewählten Patienten eine anhaltende, medikamentenfreie Remission möglich sein könnte [4, 5].
Lassen Sie uns in die rheumatologische Routineversorgung gehen und anhand von drei Fallbeispielen neue Erkenntnisse und Vorgehensweisen in der Rheumatologie veranschaulichen.
Fall 1
Ein 78-jähriger Patient stellt sich mit seit über acht Wochen bestehenden, symmetrischen Gelenkschwellungen der Hände vor. Die Beschwerden gehen mit ausgeprägten Schmerzen einher (numerische Ratingskala 7/10). Zusätzlich berichtet er über eine morgendliche Gelenksteifigkeit von etwa 90 Minuten, in dieser Zeit ist ein Faustschluss nicht möglich. Im Tagesverlauf bessern sich Schmerzen und Funktionseinschränkung unter zunehmender Mobilisierung. Die Entzündungsparameter sind erhöht (CRP 3,8 mg/dl [Norm < 0,5 mg/dl], BSG 72 mm/h). Autoimmunserologisch sind sowohl Rheumafaktor, als auch Anti-CCP-Antikörper positiv. Anamnestisch und klinisch ergeben sich keine Hinweise auf eine Infektion. Es imponieren deutlich geschwollene Handgelenke sowie MCP-Gelenke II bis IV beidseits. Arthrosonografisch zeigt sich an den betroffenen Gelenken eine floride Synovitis (Abbildung 1).
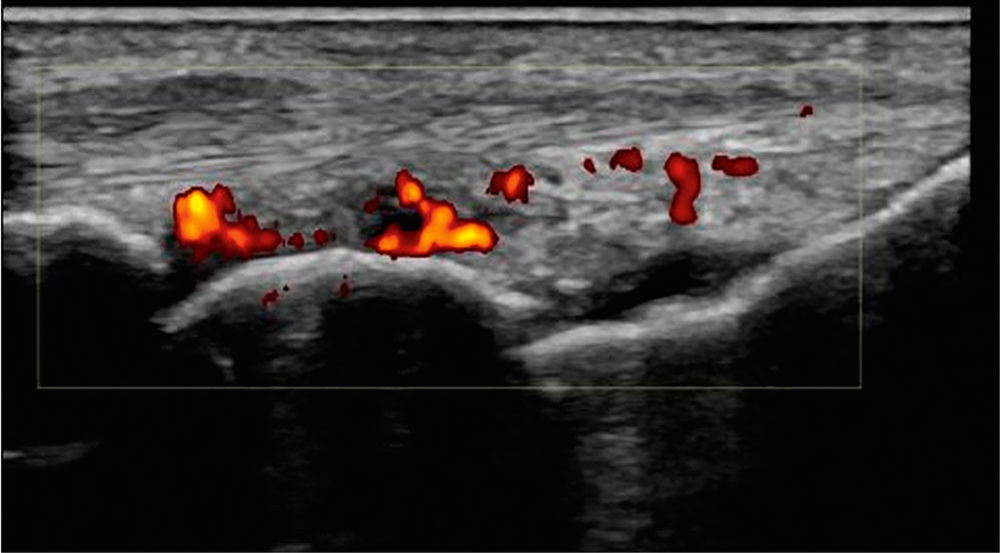
Abbildung 1: Ultraschallbefund eines Handgelenks im dorsalen Längsschnitt mit Power-Doppler-Positivität als Zeichen der Inflammation (farbliche Kodierung).
In Zusammenschau wird die Diagnose einer Late-onset-rheumatoiden Arthritis gestellt. Als medikamentöse Therapie wird leitliniengerecht mit einer krankheitsmodifizierenden Basistherapie (DMARDs) mit Methotrexat (15 mg/Woche) begonnen. Bei hohem Leidensdruck erfolgt überbrückend eine Glukokortikoidgabe, die nach einem Reduktionsschema innerhalb von drei Monaten ausgeschlichen wird [6].
Kortison so kurz wie möglich
Dauertherapien mit niedrig dosiertem Prednisolon unterhalb der sogenannten Cushing-Schwelle (< 7,5 mg/Tag) waren lange Zeit eine etablierte Behandlungsstrategie bei rheumatoider Arthritis. Insbesondere bei älteren und multimorbiden Patienten findet sich in der klinischen Praxis nicht selten eine Prednisolon-basierte Dauertherapie bis hin zur Monotherapie. Daten der Kerndokumentation (seit 1993 etabliertes deutschlandweites Versorgungsforschungsprojekt des Deutschen Rheuma-Forschungszentrums) zeigen, dass etwa ein Viertel der Betroffenen ein Jahr nach Erstdiagnose weiterhin Glukokortikoide einnimmt, wobei dieser Anteil auch nach mehr als fünf Jahren Erkrankungsdauer nahezu unverändert bleibt [7].
Inzwischen ist jedoch durch Beobachtungsstudien gut belegt, dass auch niedrig dosierte Glukokortikoide (< 5 mg Prednisolon/Tag) mit einem erhöhten Risiko glukokortikoidassoziierter Nebenwirkungen, insbesondere Infektionen, assoziiert sind [8]. 2022 veröffentlichte die European Alliance of Associations for Rheumatology (EULAR) aktualisierte Leitlinien zur rheumatoiden Arthritis, in denen betont wird, dass Glukokortikoide ausschließlich kurzfristig als Bridging-Therapie eingesetzt und spätestens nach drei Monaten vollständig abgesetzt werden sollen, um einen chronischen Gebrauch zu vermeiden [6].
Aktuelle Studiendaten zeigen zudem, dass niedrig dosiertes Prednisolon bei einem Großteil älterer Patienten auch nach längerer Anwendung kontrolliert ausgeschlichen werden kann [9]. Gleichzeitig belegen neuere Studien, dass moderne Biologika auch im höheren Lebensalter wirksam sind und insgesamt ein akzeptables Sicherheitsprofil aufweisen [10, 11]. Bei Patienten mit erhöhtem Infektionsrisiko kann der bevorzugte Einsatz von Basistherapien mit kurzer Halbwertszeit sinnvoll sein, da diese eine rasche Elimination und damit eine flexible Therapieanpassung ermöglichen.
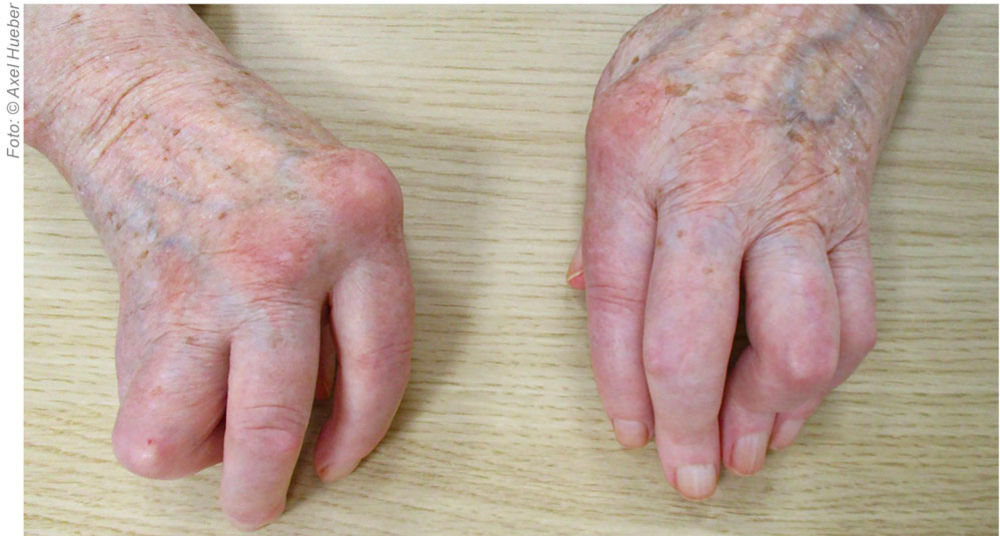
Abbildung 2: Fortgeschrittene Handdeformitäten bei langjähriger unkontrollierter rheumatoider Arthritis mit ausgeprägter Ulnardeviation der Finger, Subluxationen der MCP-Gelenke sowie daraus resultierender deutlicher funktioneller Einschränkung.
Biosimilars für biologische DMARDs
Vor diesem Hintergrund zielt die moderne Therapie der rheumatoiden Arthritis, auch im höheren Lebensalter, auf eine leitliniengerechte krankheitsmodifizierende Behandlung mit DMARDs ab, mit dem Ziel einer nachhaltigen Krankheitskontrolle ohne dauerhaften Einsatz von Glukokortikoiden. Gelenkdestruktionen, wie sie in Abbildung 2 dargestellt sind, werden somit zukünftig immer seltener anzutreffen sein. Angesichts der hohen Therapiekosten biologischer DMARDs stehen inzwischen mehrere Biosimilars zur Verfügung, die eine vergleichbare Wirksamkeit und Sicherheit aufweisen und zu einer relevanten Reduktion der Behandlungskosten beitragen können.
Fall 2
Eine 67-jährige Patientin stellt sich mit einer Einweisung ihrer Hausärztin in der Notaufnahme vor. Im Rahmen eines Routine-Check-ups waren erhöhte Entzündungsparameter aufgefallen (CRP 5,6 mg/dl [Norm < 0,5 mg/dl], BSG 95 mm/h).
Zudem bestehen seit mehreren Wochen zunehmende Schmerzen und eine ausgeprägte Kraftminderung im Schulter- und Beckengürtel. Im Alltag ist sie dadurch inzwischen deutlich eingeschränkt, so kann sie die Arme nicht mehr über den Kopf heben, benötigt beim Haarekämmen Hilfe durch ihre Tochter und auch das Aufstehen aus dem Sitzen fällt ihr zunehmend schwer. Seit wenigen Tagen bestehen außerdem zunehmende Kopfschmerzen temporal links, die als stark belastend empfunden werden. Kauschmerzen und Sehstörungen werden verneint.
Klinisch und anamnestisch ergeben sich keine Hinweise auf eine Infektion. Die Patientin wird auf die rheumatologische Normalstation aufgenommen mit der Verdachtsdiagnose einer Großgefäßvaskulitis. Noch am Aufnahmetag erfolgt eine Ultraschalluntersuchung der Temporalarterien, A. axillaris bds. als auch der Schultern. Die linke Temporalarterie weist eine deutliche Intima-Media-Verdickung auf, im Ultraschallbild sieht man ein „Halo-Zeichen“. Zusätzlich zeigt sich im Ultraschall der Bizepssehnen eine symmetrische Tendinitis. In Zusammenschau der Befunde wird die Diagnose einer Polymyalgia rheumatica (PMR) mit begleitender Riesenzellarteriitis (RZA) gestellt.
Es erfolgt eine umgehende systemische Glukokortikoidtherapie mit Prednisolon 60 mg/Tag und die Organisation einer zeitnahen ambulanten rheumatologischen Weiterbetreuung. Bei möglichem Rezidiv wird die Einleitung einer krankheitsmodifizierenden Basistherapie erwogen.
Häufige Assoziation von RZA und PMR
Der geschilderte Fall verdeutlicht exemplarisch die enge klinische und pathophysiologische Verknüpfung von PMR und RZA. Aktuelle Studien zeigen, dass bei etwa einem Fünftel der PMR-Patienten bereits bei Diagnosestellung eine begleitende RZA vorliegt, während umgekehrt ein erheblicher Anteil der RZA-Betroffenen PMR-Symptome aufweist [12, 13].
Temporalarterienbiopsie nur noch selten erforderlich
In den aktuellen EULAR-Empfehlungen von 2022 hat die Temporalarterienbiopsie als invasives Verfahren deutlich an Bedeutung verloren. Bei klinischem Verdacht auf eine kraniale RZA wird heute zunächst eine nicht-invasive Bildgebung empfohlen, allen voran der Ultraschall der Arteria temporalis und axillaris, der in erfahrenen Händen eine hohe diagnostische Aussagekraft besitzt (Abbildung 3). Alternativ können, je nach Verfügbarkeit und Fragestellung, auch eine FDG-PET-CT oder eine MRT-Angiografie zur Beurteilung kranialer und extrakranieller Gefäße eingesetzt werden [14].
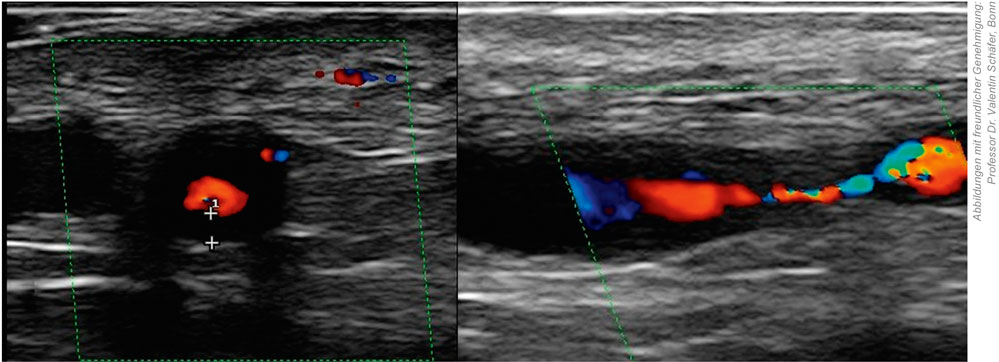
Abbildung 3: Typischer Ultraschallbefund bei Riesenzellarteriitis mit „Halo-Zeichen“ der Arteria temporalis (links) und lumeneinengender Stenose der Arteria temporalis communis (rechts).
IL-6-Blockade und JAK-Inhibitoren bei refraktären Verläufen
Therapeutisch hat sich bei PMR und RZA in den vergangenen Jahren ebenfalls viel getan. Lange Zeit war Prednisolon bei der RZA die einzige wirksame Therapieoption. Seit 2017 ist mit Tocilizumab erstmals ein Interleukin-6-Rezeptor-Inhibitor in der EU für die Behandlung der RZA zugelassen. Durch die Hinzunahme von Tocilizumab lässt sich eine deutliche Reduktion (kumulativ ca. 2 g Glukokortikoidreduktion) der Steroiddosierung erreichen [15]. Eine bekannte Einschränkung der IL-6-Blockade bleibt, dass CRP zur Verlaufskontrolle nicht mehr zuverlässig nutzbar ist. Neu hinzugekommen ist 2025, nach positiven Ergebnissen der SELECT-GCA-Studie, die Zulassungserweiterung für den JAK-Inhibitor Upadacitinib – ein orales Immunsuppressivum aus der Gruppe der Janus-Kinase (JAK)-Inhibitoren, das entzündliche Signalwege (speziell JAK1) hemmt – bei RZA [16]. Aufgrund eines Rote-Hand-Briefes aus dem Jahr 2023, der alle JAK-Inhibitoren in der Rheumatologie betrifft, ist der Einsatz von Upadacitinib aktuell auf ausgewählte Patienten beschränkt, bei denen keine geeigneten Therapiealternativen bestehen 1. Auch bei der PMR gibt es Neuerungen: Mit Sarilumab steht seit 2024 ein weiterer IL-6-Rezeptor-Inhibitor zur Verfügung, der für die therapierefraktäre PMR zugelassen und inzwischen in die aktuelle S2e-Leitlinie aufgenommen wurde [17, 18].
1 Bei Patienten mit rheumatoider Arthritis (RA), die bestimmte Risikofaktoren aufwiesen und mit JAK-Inhibitoren behandelt wurden, wurde eine erhöhte Inzidenz von malignen Erkrankungen, schwerwiegenden unerwünschten kardiovaskulären Ereignissen (MACE), schwerwiegenden Infektionen, venösen Thromboembolien (VTE) und Mortalität im Vergleich zu TNF-alpha-Inhibitoren beobachtet. www.bfarm.de/SharedDocs/Risikoinformationen/Pharmakovigilanz/DE/RHB/2023/rhb-januskinase.html
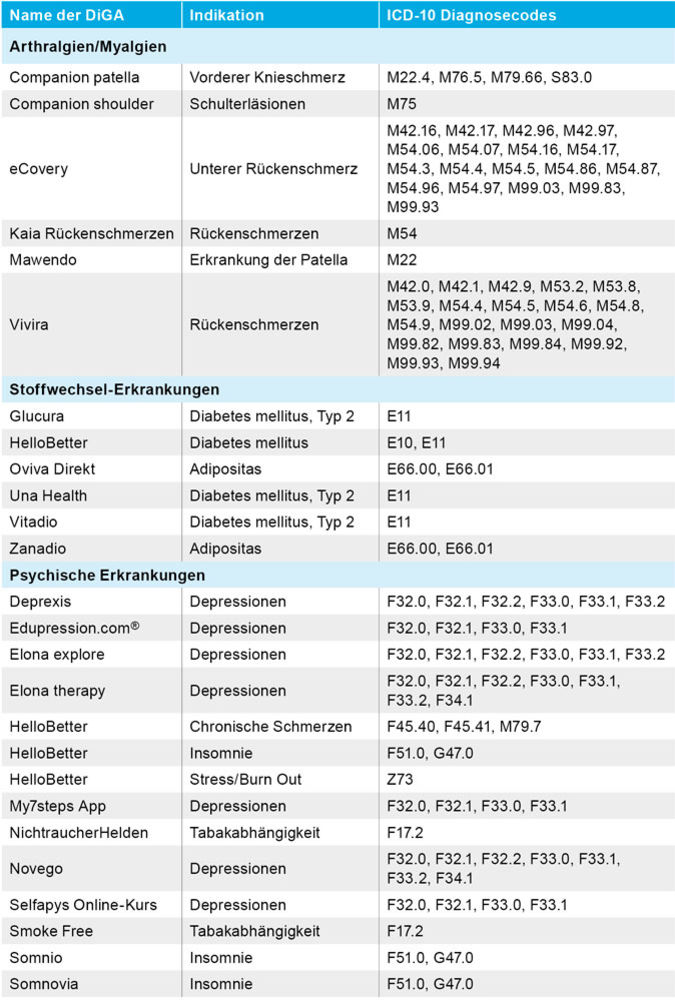
Tabelle 1: Übersicht ausgewählter Digitaler Gesundheitsanwendungen (DIGA) aus dem DiGA-Verzeichnis des Bundesinstituts für Arzneimittel und Medizinprodukte (BfArM), Stand 1/2026.
Fall 3
Eine 46-jährige Patientin mit seit zwei Jahren bekannter seropositiver rheumatoider Arthritis stellt sich zur regulären Verlaufskontrolle in der rheumatologischen Ambulanz vor. Zu Beginn der Erkrankung war aufgrund einer hohen Krankheitsaktivität mehrfach eine systemische Glukokortikoidtherapie notwendig gewesen. Unter der seit Erstdiagnose bestehenden Basistherapie mit Methotrexat 25 mg/Woche ist die Erkrankung aktuell gut kontrolliert.
Anamnestisch besteht ein langjähriger Nikotinkonsum von etwa 25 pack-years. Als Vorerkrankungen sind unter anderem eine arterielle Hypertonie, Hypercholesterinämie und Adipositas bekannt. Zur Dauermedikation zählen unter anderem Ramipril, Amlodipin und Rosuvastatin.
Im Rahmen der Vorstellung erfolgt ein routinemäßiges Screening auf Begleiterkrankungen. Die Blutdruckwerte sind normoton, ein Depressions-Screening bleibt unauffällig. Bereits beim vorherigen rheumatologischen Termin war ein kardiovaskulärer Risikoscore erhoben worden, woraufhin bei Hypercholesterinämie die Statintherapie intensiviert wurde.
Bei bekannter Adipositas wurde zuletzt eine digitale Gesundheitsanwendung zur Gewichtsreduktion verordnet. Die Patientin berichtet über eine erfolgreiche Ernährungsumstellung mit erster Gewichtsabnahme. Auf ihren Wunsch hin wird ergänzend eine DiGA zur Tabakentwöhnung verordnet. Abschließend wird der Impfstatus überprüft und für die kommende Wintersaison eine Influenza- sowie eine COVID-19-Impfung empfohlen.
Hoher Stellenwert von Begleiterkrankungen
Der dargestellte Fall zeigt exemplarisch, dass bei Patienten mit rheumatoider Arthritis, neben der Kontrolle der entzündlichen Aktivität, Begleiterkrankungen zunehmend eine zentrale Rolle spielen. Chronische systemische Entzündungen und medikamentöse Therapien begünstigen eine Vielzahl von Komorbiditäten wie beispielsweise Herz-Kreislauf-Erkrankungen, Infektionen, Depression und beeinflussen Prognose, Lebensqualität und Mortalität maßgeblich [19, 20, 21]. Dabei stellen Herz-Kreislauf-Erkrankungen die häufigste Todesursache bei Patienten mit entzündlich-rheumatischen Erkrankungen dar und treten unabhängig von klassischen Risikofaktoren vermehrt auf [22, 23]. Neben häufigen Faktoren wie Nikotinabusus, Hypertonie oder Dyslipidämie trägt insbesondere die chronische systemische Inflammation wesentlich zur Atherosklerose und Plaque-Instabilität bei [24]. Entsprechend gilt die konsequente Kontrolle der Krankheitsaktivität gemeinsam mit der Optimierung kardiovaskulärer Risikofaktoren als zentraler Bestandteil der Prognoseverbesserung bei rheumatischen Erkrankungen.
Neue Impfempfehlungen bei entzündlich-rheumatischen Erkrankungen
Infektionen sind eine weitere häufige Begleiterkrankung entzündlich-rheumatischer Erkrankungen. Patienten mit rheumatoider Arthritis haben ein deutlich erhöhtes Risiko für schwere Infektionen, das bei hoher Krankheitsaktivität weiter ansteigt [25]. Neben den STIKO-Empfehlungen existieren seit 2025 auch aktuelle Empfehlungen der Deutschen Gesellschaft für Rheumatologie und Immunologie (DGRh) zur Impfung bei entzündlich-rheumatischen Erkrankungen, die den erweiterten Impfschutz im Kontext immunsuppressiver Therapien adressieren [26, 27]. So werden für erwachsene Patienten mit entzündlich-rheumatischen Erkrankungen unter immunsuppressiver Therapie unter anderem jährliche Impfungen gegen Influenza und COVID-19 sowie ein vollständiger Impfschutz gegen Pneumokokken empfohlen. Seit Ende 2025 empfiehlt die STIKO zudem die Herpes-zoster-Impfung bereits ab dem 18. Lebensjahr für diese Patientengruppe und nicht mehr erst ab dem 50. Lebensjahr. Ärztliche Empfehlungen erhöhen dabei nachweislich die Impfbereitschaft [28].
Neue Studien zur und Bedeutung von Depressionen
Auch Depressionen treten bei Betroffenen mit entzündlich-rheumatischer Erkrankungen mit einem etwa 1,5- bis 2-fach erhöhten Risiko auf [29]. Sie sind klinisch bedeutsam, da sie das Therapieansprechen der rheumatischen Grunderkrankung negativ beeinflussen können. Neue Register- und Studiendaten zeigen, dass Patienten, die depressive Symptome aufweisen eine geringere Wahrscheinlichkeit haben, eine niedrige Krankheitsaktivität zu erreichen [30].
Digitale Gesundheitsanwendungen
Seit 2020 besteht in Deutschland die Möglichkeit, digitale Gesundheitsanwendungen (DiGA) als „Apps auf Rezept“ zu verordnen, sie sind als geprüfte Medizinprodukte erstattungsfähig und können das Management häufiger Begleiterkrankungen wie Nikotinabhängigkeit, Adipositas oder Depression evidenzbasiert unterstützen [31]. Stand Januar 2026 sind im DiGA-Verzeichnis des Bundesinstituts für Arzneimittel und Medizinprodukte (BfArM) 58 digitale Gesundheitsanwendungen gelistet. Auch wenn bislang keine DiGA explizit für entzündlich-rheumatische Erkrankungen zugelassen ist, eignen sich zahlreiche Anwendungen für das strukturierte Management häufiger Begleiterkrankungen (Tabelle 1).

Die Autoren erklären, dass sie keine finanziellen oder persönlichen Beziehungen zu Dritten haben, deren Interessen vom Manuskript positiv oder negativ betroffen sein könnten.
Das Literaturverzeichnis kann im Internet unter www.bayerisches-aerzteblatt.de (Aktuelles Heft) abgerufen werden.
Autorin und Autor

Professor Dr. Dr. Axel J. Hueber 1, 2
1 Abteilung Rheumatologie, Klinik für Innere Medizin 5, Klinikum Nürnberg, Universitätsklinik der Paracelsus Medizinischen Privatuniversität, Nürnberg
2 Rheumazentrum Erlangen-Nürnberg e. V., Erlangen
Teilen:
Das könnte Sie auch interessieren: